Sekrece a složení žluče
Žluč se tvoří v hepatocytech a je vylučována přes žlučové kapiláry, malé žlučovody, velké žlučovody (běží s lymfatiky, větvemi portální žíly a větvemi a. hepatica), které se spojují v levý a pravý jaterní žlučovod, tyto v ductus hepaticus communis, do kterého ústí ductus cysticus a vytváří ductus choledochus (často do něj ústí hlavní pankreatický vývod), který končí v duodenu Vaterskou papilou.
Jaterní žluč je izotonická tekutina s elektrolytovým složením podobným krevní plazmě (celková koncentrace solutů je 30 – 40 g/l). Žluč ve žlučníku je již zcela jiného složení, protože se většina anorganických iontů i bikarbonátu zpětně resorbuje přes žlučníkový epitel (celková koncentrace solutů je 100 – 150 g/l). Hlavními solubilními složkami žluči jsou
- žlučové kyseliny (80 %)
- lecitin a stopy jiných fosfolipidů (16 %)
- cholesterol (4 %, při litogenních stavech se hodnota cholesterolu zvyšuje na 8 – 10 %)
Ostatními složkami jsou: konjugovaný bilirubin, proteiny (imunoglobuliny, albumin, metabolity hormonů), elektrolyty, hlen a často léky a jejich metabolity.
Celková bazální sekrece jaterní žluče je 500 – 600 ml. Kanalikulární membrána hepatocytů je tvořena mikroklky, které obsahují kontraktilní elementy. Před vyloučením do žluče je mnoho látek zpětně vstřebáno do hepatocytů, zatímco fosfolipidy, část primárních žlučových kyselin a cholesterolu jsou primárně syntetizovány v hepatocytech.
Mezi mechanismy regulující vznik žluči patří aktivní transport žlučových kyselin z hepatocytu do žlučových kapilár, aktivní transport ostatních anorganických aniontů a cholangiocelulární sekrece (cAMP dependentní sekrece sodíku a tekutiny bohaté na bikarbonát do žlučovodu regulována sekretinem).
Transport žlučových komponent z portální krve do žlučových kapilár je umožněn transportéry na obou pólech hepatocytu:
- bazolaterální strana umožňuje transport z portální krve do hepatocytu:
- NTCP – Na+/taurocholát kotransportér.
- OATPs – proteiny transportující organické anionty.
- kanalikulární strana umožňuje transport z hepatocytu do žluče:
- F1C1 – aminofosfolipid transferáza „flipáza“, která je důležitá k zachování asymetrie v koncentraci lipidů v hepatocytu a primární žluči. Defektní u progresivní familiární intrahepatální cholestáze typ 1 (PFIC1) a benigní rekurentní intrahepatické cholestáze typ 1 (BRIC1) a způsobuje nefunkčnost i všech ostatních ATP dependentních transportérů.
- BSEP (bile salt export pumps), defektní u progresivní familiární intrahepatální cholestázy typ 2 (PFIC2) a benigní rekurentní intrahepatické cholestáze typ 2 (BRIC2).
- MDR3 – fosfolipidový transportér, defektní u progresivní familiární intrahepatální cholestázy typ 3 (PFIC3).
- MRP2 (anionic conjugate export pump), zprostředkuje exkreci různých konjugátů, které vznikají ve fázi II konjugace (bilirubin mono- a diglukuronid, léky). Jeho mutace působí Dubin-Johnsonův syndrom s konjugovanou hyperbilirubinémií.
- MDR1 (multidrug resistance), transportuje hydrofobní kationické sloučeniny.
- ABCG5/G8 – dva hemitransportéry, které fungují jako pár. Umožňují transport cholesterolu a fytosterolu do žluče. Defektní u sitosterolémie.
- AE2 (anion exchanger isoform 2) – Cl/HCO3 ATP-independentní transportér umožňující žlučovou sekreci bikarbonátu
- CFTR – cystic fibrosis transmembrane regulator, je lokalizovaný v epitelu žlučovodů (ale ne na žlučovém pólu hepatocytů!). Je defektní při cystické fibróze, což působí postižení regulace cholangiocelulárního pH během formace žluče s následnou chronickou cholestázou až biliární cirhózou.
Žlučové kyseliny – primární žlučové kyseliny (cholová a chenodeoxycholová) jsou syntetizovány z cholesterolu v játrech, konjugované s glycinem nebo taurinem a vylučovány do žluče. U zdravých jedinců je poměr konjugátů glycinu a taurinu 3:1. Sekundární žlučové kyseliny (deoxycholová a litcholová) se tvoří v tlustém střevě z primárních žlučových kyselin činností baktérií. Kyselina deoxycholová je ze střeva mnohem více reabsorbována než litcholová. Dále je možno najít v nízké koncentraci kyselinu ursodeoxycholovou a stereoizomer kyseliny chenodeoxycholové. Funkce:
- slouží jako detergenty, které ve vodných roztocích a nadkritické koncentraci (˃ 2 mmol/l) tvoří agregáty zvané micely. Cholesterol je jen málo rozpustný ve vodě, jeho rozpustnost ve žluči závisí zejména na koncentraci žlučových kyselin a fosfatidilcholinu. Normální složení favorizuje tvorbu rozpustných smíšených micel, zatímco při abnormálním složení cholesterol precipituje ve formě cholesterolových krystalů.
- usnadňují střevní absorpci tuku v potravě cestou micelárního transportu (zejména cholesterolu a vitamínů rozpustných v tucích).
- slouží jako hlavní regulátor tvorby žluče játry a pomáhají transportu vody a elektrolytů v tenkém i tlustém střevě.
Enterohepatální cirkulace – nekonjugované a v menší míře i konjugované žlučové kyseliny jsou absorbovány pasivní difuzí z celého střeva (nejvíce z distálního ilea). Reabsorbované žlučové kyseliny vstupuji do portální krve a jsou transportovány k hepatocytům, zde rekonjugovány a znovu vyloučeny do žluče. Normální pool žlučových kyselin je 2 – 4 gramy. Účinnost střevní absorpce je cca 95 %. Denně dochází ke ztrátě 0,2 – 0,4 g žlučových kyselin stolicí, která je kompenzována jejich jaterní syntézou. Maximální kapacita syntézy žlučových kyselin je cca 5 g/den. Při poruše jejich vstřebávání tato syntéza nemusí pokrývat ztráty. Žlučové kyseliny, které se vrací do jater portální krví inhibují jaterní syntézu primárních žlučových kyselin de novo:
- inhibicí cholesterol-7-hydroxylázy.
- jaterní BSEP je upregulován pomocí FXR (famesoidní X receptor), což je sensor žlučových kyselin, který také inhibuje syntézu žlučových kyselin
- exprese cholesterolového transportéru ABCG5/G8 je upregulována jaterním X receptorem (LXR), který slouží jako senzor oxysterolu
Během trávení potravy podstupuje pool žlučových kyselin nejméně jeden enterohepatický cyklus (počet závisí na množství a složení potravy). Průměrně během jednoho dne dojde k 5 -10 cyklům.
Žlučník a funkce svěračů – v lačném stavu brání Oddiho svěrač toku žluče z ductus choledochus do duodena. Tento vysoký tonus slouží k:
- 1. Prevenci refluxu obsahu z duodena do pankreatického vývodu a žlučovodu.
- 2. Podpoře plnění žlučníku.
Hlavním regulátorem evakuace žlučníku je peptidový hormon cholecystokinin, který je uvolňován sliznicí duodena jako odpověď na trávení potravy s vysokým obsahem tuku a aminokyselin. Cholecystokinin působí silnou kontrakci žlučníku a zároveň relaxaci Oddiho svěrače.
Jaterní žluč je v žlučníku pomocí ATP dependentní resorpce vody a elektrolytů zahuštěna. Téměř celý pool žlučových kyselin může být při nočním lačnění ve žlučníku sekvestrován a uvolněn do duodena během prvního jídla dne. Průměrná kapacita žlučníku je cca 30 ml žluče.
Choroby žlučníku
Vrozené anomálie žlučníku
Nejsou vzácné a počítá se mezi ně abnormality v počtu, velikosti a tvaru žlučníku. Může být určitá predispozice k akutní torzi, volvulu nebo herniaci žlučníku.
Frýgická čapka – klinicky neškodná anomálie, kdy je fundus od těla žlučníku částečně nebo úplně oddělen septem.
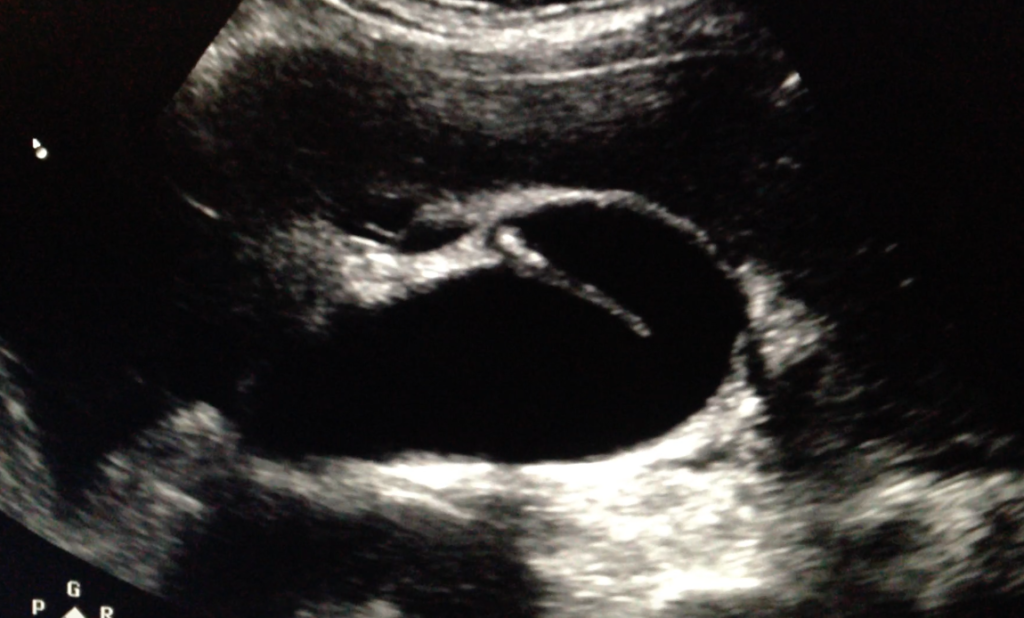
Cholecystolitiáza
Epidemiologie – v Evropě postihuje nejméně 20 % populace (zejména ve vyspělých zemích), u 30 % je někdy během života symptomatická.
Klasifikace
- 1. Cholesterolové kameny ˃ 90 – 95 % všech konkrementů (obsahují více než 50 % cholesterol monohydrátu + kalciové soli, žlučové pigmenty a proteiny.
- 2. Pigmentové kameny < 10 % všech konkrementů. Složeny zejména z kalcium bilirubinátu, obsahují méně než 50 % cholesterolu. Dělí se dále na:
- černé pigmentové – u pacientů s chronickou hemolýzou nebo cirhózou.
- hnědé pigmentové – nevznikají ve žlučníku, ale v choledochu u pacientů po cholecystektomii, u nemocných s primární sklerotizující cholangitidou či chronickou cholangoitidou.
Rizikové faktory
- obezita vyšší BMI i diabetes mellitus II. typu jsou rizikovým faktorem vzniku cholesterolové litiázy zejména u žen.
- inaktivita – pravidelná fyzická aktivita riziko litiázy snižuje (hyperinzulinemie zvyšuje sekreci cholesterolu do žluče a pravidelné cvičení snižuje hladinu inzulinu.
- nepravidelné stravování a dieta – nepravidelná strava má za následek nepravidelné vyprazdňování žlučníku. Dle některých studií má protektivní vliv ovoce a zelenina, vitamín C.
| Cholesterolové konkrementy | |
| 1. demografické a genetické faktory | prevalence nejvyšší – Severoameričtí Indiáni, Chile, nižší Severní Evropa, ještě nižší Asie, nejnižší Japonsko. |
| 2. obezita, metabolický syndrom | normální pool žlučových kyselin, ale hypersaturace cholesterolem. |
| 3. hmotnostní úbytek | mobilizace tkáňového cholesterolu vede k hypersaturaci žluče cholesterolem a snížení enterohepatické cirkulace. |
| 4. vysokoenergetická, tučná dieta | |
| 5. ženské pohlavní hormony | stimulace jaterních lipoproteinových receptorů, zvýšení střevní resorpce a žlučové sekrece cholesterolu, snížení sekrece žlučových kyselin, snížení konverze cholesterolu na jeho estery |
| 6. vyšší věk | zvýšení biliární sekrece cholesterolu, snížení poolu žlučových kyselin, snížení sekrece žlučových solí |
| 7. dlouhodobá parenterální výživa | ↘ |
| 8. těhotenství | → hypomotilita žlučníku |
| 9. hladovění | ↗ |
| 10. léky | octreotid – hypomotilita žlučníku, clofibrat – zvýšená biliární sekrece cholesterolu |
| 11. snížená sekrece žlučových kyselin | Primární biliární cirhóza |
| Defekt genu CYP7A1 | |
| 12. snížená sekrece fosfolipidů | Defekt genu MDR3 |
| 13. poranění míchy | |
| Pigmentové konkrementy | |
| 1. demografické a genetické faktory | Asie |
| 2. chronická hemolýza | |
| 3. perniciózní anémie | |
| 4. alkoholická cirhóza | |
| 5. cystická fibróza | |
| 6. chronická infekce biliárního traktu | |
| 7. vyšší věk | |
| 8. choroba, resekce nebo bypass ilea |
Cholesterolové konkrementy
Cholesterol je nerozpustný ve vodě, ke vzniku disperze jsou proto potřeba micely nebo vezikuly. Cholesterol a fosfolipidy jsou vylučovány do žluče jako vezikuly tvořené dvouvrstvou, které se mění ve smíšené micely obsahující žlučové kyseliny, fosfolipidy a cholesterol. Při převaze cholesterolu nad fosfolipidy a žlučovými kyselinami zůstávají vezikuly nestabilní, spojují do mnohovrstevných vezikul, ze kterých precipitují cholesterolové krystaly.
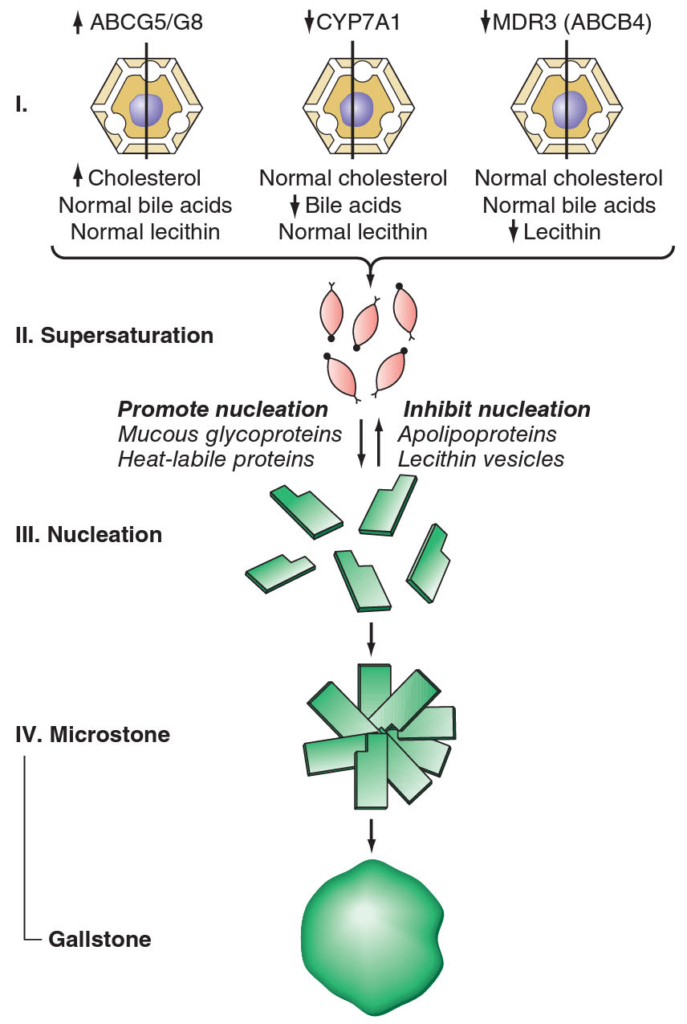
Mechanismy a rizikové faktory tvorby litogenní žluči:
- 1. Zvýšená biliární sekrece cholesterolu – u pacientů se žlučovými kameny zvyšuje biliární sekreci cholesterolu jeho příjem v potravě. Toto ovšem neplatí u pacientů bez cholecystolitiázy. Hypersaturace žluče je způsobená:
- zvýšeným vylučováním cholesterolu – při obezitě, metabolickém syndromu, vysokoenergetické dietě nebo dietě bohaté na cholesterol, po lécích (např. clofibrát), při zvýšené aktivitě hydroxymetylglutaryl-koenzym A reduktázy (HMG-CoA) a zvýšeném jaterním příjmu cholesterolu z krve.
- bodovým nukleotidovým polymorfismem genu pro transportér cholesterolu ABCG5/G8 (nalezen u 21 % pacientů se žlučníkovými konkrementy, ale jen u 9 % zdravé populace) působí hyperaktivaci tohoto transportéru a následnou hypersaturaci žluči cholesterolem.
- nízkým vylučováním žlučových kyselin a fosfolipidů.
- mutací genu CYP7A1 s deficitem cholesterol 7-hydroxylázy, která katalyzuje počáteční krok konverze cholesterolu na žlučové kyseliny. Homozygoti trpí hypercholesterolémií a zvýšenou incidencí cholesterolových konkrementů.
- mutací genu MDR3, který kóduje fosfolipidový transportér na žlučovém pólu hepatocytu se snížením sekrece fosfolipidů do žluče, což má za následek její hypersaturaci cholesterolem.
- zvýšenou konverze kyseliny cholové na deoxycholovou díky její zvýšené dehydroxylaci. Nově vzniklá kyselina deoxycholová je zvýšeně absorbována a její hypersekrece je spojena s hypersekrecí cholesterolu do žluče.
- zvýšeným vylučováním cholesterolu – při obezitě, metabolickém syndromu, vysokoenergetické dietě nebo dietě bohaté na cholesterol, po lécích (např. clofibrát), při zvýšené aktivitě hydroxymetylglutaryl-koenzym A reduktázy (HMG-CoA) a zvýšeném jaterním příjmu cholesterolu z krve.
- 2. Zvýšená nukleace krystalů cholesterol monohydrátu – způsobena nadbytkem pronukleačních faktorů (mucin, imunoglobuliny) nebo nedostatkem antinukleačních faktorů (apo A-I a A-II). Cholesterolová jádra i krystaly rostou na mucinové vrstvě.
- 3. Hypomotilita žlučníku – konkrementy vznikají, pouze pokud se žlučník nevyprázdní úplně. Velká část pacientů s cholecystolitiázou má anomálii ve vyprazdňování žlučníku (zvýšený objem žlučníku jak při lačnění tak po testovacím jídle).
- 4. Těhotenství – sludge se objevuje u 20 – 30 % a konkrementy u 5 – 12 % těhotných žen, protože v těhotenství se zvyšuje saturace žluče cholesterolem (zejména během 3. trimestru) a nedochází k úplnému vyprazdňování žlučníku při jídle. Po porodu dochází k rychlé normalizaci. Sludge bývá velice často asymptomatický a rozpouští se brzy po porodu. Litiáza je často spojena s biliární kolikou, přesto se po porodu konkrementy mohou také rozpustit.
- 5. Nízkoenergetická dieta – u 10 – 20 % pacientů s rapidním úbytkem hmotnosti při nízkoenergetické dietě, se objevuje cholecystolitiáza, výrazně protektivním opatřením může být podání kyseliny ursodeoxycholové.
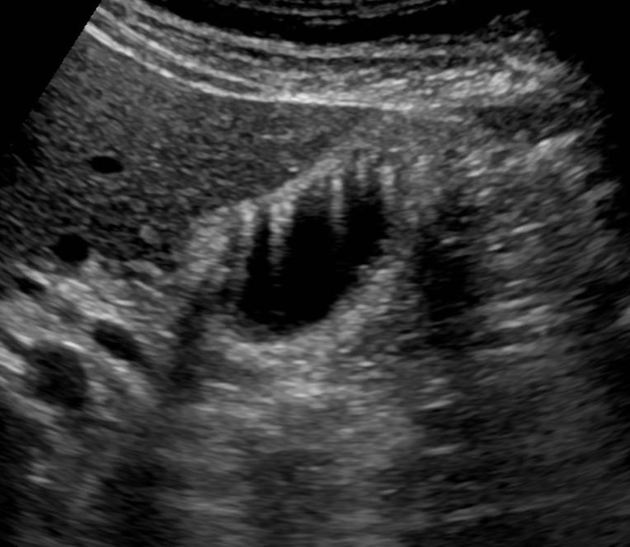
Sludge je hrubý, mukózní materiál, který obsahuje tekuté krystaly z lecitinu a cholesterolu, solidní krystaly cholesterol monohydrátu, kalcium bilirubinát a mucin. Vždy znamená hypersaturaci žluče buď cholesterolem nebo kalcium bilirubinátem. Typicky tvoří srpovitou vrstvu v nejnižších částech žlučníku a při ultrasonografii vytváří charakteristická echa. Jeho přítomnost podmiňují dvě abnormality a to porušení rovnováhy mezi sekrecí a eliminací mucinu a již přítomná nukleace žlučníkových komponent. Sludge je často spojen s abnormalitami při kterých dochází k hypomotilitě žlučníku (stav po chirurgických výkonech, popáleniny, totální parenterální výživa, těhotenství, perorální antikoncepce). Tyto stavy jsou také spojeny s vyšším rizikem cholecystolitiázy. Sludge může být prekurzorem cholecystolitiázy.
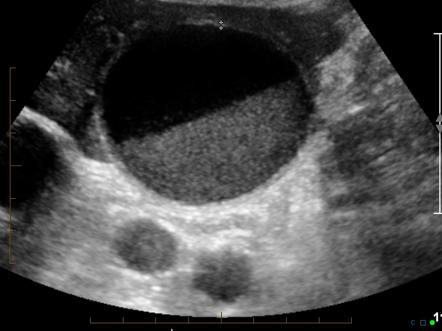
Pigmentové konkrementy
Nejčastější vznikají u Asiatů, často jsou spojeny s chronickou infekcí žlučníku a žlučových cest.
Černé konkrementy – jsou tvořeny kalcium bilirubinátem nebo komplexy s kalciem a mucinózními glykoproteiny. Nejčastěji u pacientů s chronickou hemolýzou, jaterní cirhózou, Gilbertovým syndromem, cystickou fibrózou a chorobami ilea (resekce nebo bypass).
Hnědé konkrementy – tvořeny kalcium bilirubinátem s různým množstvím cholesterolu a proteinů. Způsobeny přítomností zvýšeného množství nekonjugovaného bilirubinu ve žluči, který precipituje a tvoří konkrementy. Ke spontánní dekonjugaci nadbytečného množství rozpustných mono- a diglukuronidů (zprostředkováno endogenními β-glukuronidázami) může dojít při chronické infekci žlučových cest
Klinický obraz – při migraci konkrementu do ductus cysticus nebo choledochus jsou přítomny příznaky zánětu nebo obstrukce. Při obstrukci je snaha o vypuzení konkrementu opakovanými biliárními kontrakcemi, zvyšuje se intraluminální tlak a dilatuje žlučovod. Vzniká výrazná, trvalá viscerální bolest nebo pocit plnosti v epigastriu či pravém podžebří s častou iradiací do pravého ramene, lopatky nebo mezilopatkové oblasti.
Nejcharakterističtějším příznakem je biliární kolika. Vzniká často náhle a trvá od 15 minut do 5 hodin s následným vymizením různou rychlostí. Je častěji trvalá než intermitentní (proto je kolika nepřesné pojmenování) a často provázena nauzeou a zvracením. Vznik biliární koliky může být vyprovokován tučným jídlem, požitím velkého množství potravy po epizodě dlouhého hladovění, ale i normální porcí normálního jídla. Vzniká často i v noci, několik hodin po ulehnutí. Při elevaci bilirubinu a ALP je nutné vyloučit konkrement v ductus choledochus.
CAVE Při trvání bolestivosti déle než 5 hodin je nutné vyloučit akutní cholecystitidu.
Při horečce s třesavkou a biliárními bolestmi je vždy nutné vyloučit komplikace (akutní cholecystitidu, pankreatitidu nebo cholangitidu).
Cholecystolitiáza je často dlouhodobě asymptomatická. Dle studií je u němých cholecystolitiáz riziko vzniku komplikací 10 % za 5 let, 15 % za 10 let a 18 % za 15 let. Dále bylo zjištěno, že kumulativní mortalita pro němou cholecystolitiázu je velmi malá a proto není indikována profylaktická cholecystektomie. Komplikace, které vyžadují cholecystektomii jsou mnohem častější u symptomatických pacientů. Čím je pacient v době stanovení diagnózy mladší, tím je riziko komplikací vyšší. Diabetici s cholecystolitiázou mají poněkud vyšší riziko septických biliárních komplikací.
Mirizziho syndrom – vzácná komplikace kdy je konkrement zaklíněn v krčku žlučníku nebo ductus cysticus, utlačuje ductus choledochus a působí jeho obstrukci a ikterus. Sonografie v tomto případě ukazuje konkrement, který se nachází mimo ductus choledochus. Diagnózu lze potvrdit ERCP, PTC nebo MRCP (průkaz extramurální komprese). Léčbou je provedení cholcystektomie a odstranění ductus cysticus s konkrementem. Předoperační průkaz Mirizziho syndromu je důležitý pro prevenci poranění ductus choledochus.
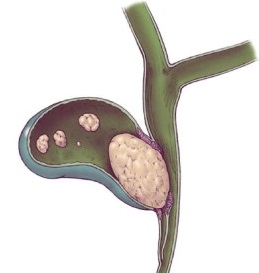
Diagnostika
| Výhody | Nevýhody | Poznámky |
| ULTRAZVUK | ||
| rychlost | limitace střevním plynem, obezitou, ascitem | metoda první volby |
| senzitivita 96 – 98 % | ||
| detekce konkrementů cca 1,5 mm | ||
| real time vyšetření (vyprazdňování žlučníku apod.) | ||
| není limitace těhotenstvím nebo ikterem | ||
| NATIVNÍ RTG BŘICHA | ||
| nízká cena | nízká senzitivita | patognomonické při kalciových konkrementech, žluči s vysokým obsahem kalcia, porcelánovém žlučníku, emfyzematózní cholecystitidě a biliárním ileu |
| rychlá dostupnost | kontraindikace v těhotenství | |
| RADIOIZOTOPOVÉ METODY (HIDA, DIDA apod.) | ||
| přesná identifikace obstrukce ductus cysticus | kontraindikace v těhotenství | |
| současné hodnocení žlučovodů | nutnost sérového bilirubinu > 103 μmol/l | |
| nízká rozlišovací schopnost | indikován ke konfirmaci suspektní akutní cholecystitidy, méně senzitivní u chronické cholecystitidy, užitečný u akalkulózní cholecystopatie, zejména při hodnocení vyprázdnění po aplikaci cholecystokininu |
Ultrasonografie – nejjednodušší vyšetření, které detekuje již kamínky průměru 1,5 mm, jeho specifita vyšetření je cca 96 – 98 %. Konkrementy tvoří akustický stín, který se mění polohou pacienta, sludge se odlišuje od konkrementů absenci akustického stínu. Lze využít i k vyšetření vyprazdňovací funkce žlučníku
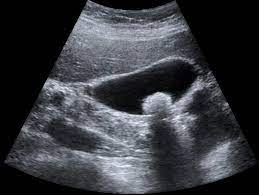
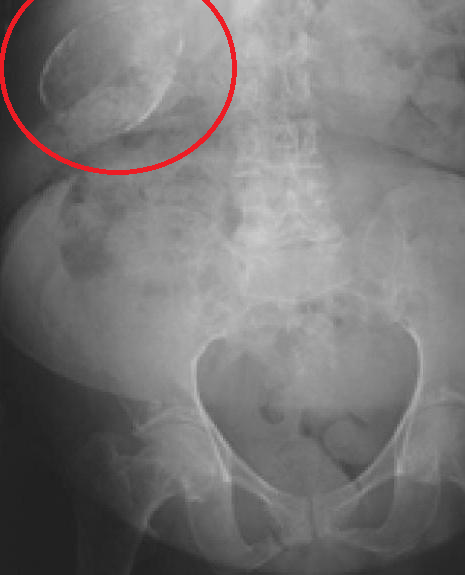
Nativní RTG břicha – aby byly konkrementy radiokontrastni, je nutný obsah dostatečného množství kalcia (10 – 15 % cholesterolových, 50 % pigmentových kamenů). Lze prokázat emfyzematózní cholecystitidu, porcelánový žlučník, žluč s vysokým obsahem kalcia („limy bile“), biliární ileus.
Radioizotopové metody – podává se 99mTechneciem značená N-substituovaná iminodioctová kyselina (IDA), která je rychle vstřebána z krve a vylučována do žluče (nutná přítomna úroveň bilirubinu > 103 μmol/l). Při nezobrazení žlučníku při normální vizualizaci žlučových cest vzniká podezření na obstrukci ductus cysticus, akutní nebo chronickou cholecystitidu nebo st. p. cholecystektomii. Ideální pro potvrzení akutní cholecystitidy.
Terapie
Chirurgická terapie – při asymptomatické cholecystolitiáze je riziko komplikací, které vyžadují chirurgický zákrok velice malá (1 – 2 % ročně). Proto profylaktická cholecystektomie není u asymptomatických pacientů indikována. Pokud lze, je preferován laparoskopický přístup. Indikace cholecystektomie:
- Přítomnost tak výrazných symptomů, že omezují pacienta v běžném životě.
- Přítomnost komplikací (anamnéza akutní cholecystitidy, pankreatitidy, píštěle atd.).
- Přítomnost jiných patologií, které zvyšují riziko komplikací (porcelánový žlučník, anamnéza akutní cholecystitidy).
- Relativní indikací – přítomnost velkých konkrementů (> 3 cm) ve vrozeně malformovaném žlučníku.
Farmakoterapie (rozpuštění konkrementů) – ursodeoxycholová kyselina v dávce 10 – 15 mg/kg/den, snižuje koncentraci cholesterolu ve žluči, dále podporuje vznik lamelární, tekuté krystalické fáze, což umožňuje lepší disperzi cholesterolu z konkrementů. Dále zpomaluje nukleaci cholesterolových krystalů. U pečlivě indikovaných pacientů (radiokontrastní litiáza, dobrá motilita žlučníku, konkrementy velikosti < 1 cm) může být disoluce úspěšná až v 50 % (během doby 6 měsíců až 2 let). Čím je konkrement menší, tím je disoluce úspěšnější. Pro tuto terapii jsou kandidáti cca 10 % symptomatických pacientů. Problémem je častá rekurence konkrementů (cca 50 % pacientů za 5 let). Tato metoda je vyhrazena pro pacienty s rekurencí choledocholitiázy po cholecystektomii a lidi, kteří z různých důvodů odmítají chirurgický výkon.
Akutní cholecystitida
Etiologie – akutní zánět žlučníku většinou následuje po obstrukci ductus cysticus konkrementem. Zánět může být způsoben třemi faktory:
- Zvýšení intraluminálního tlaku s následnou distenzí a ischemizací stěny.
- Chemické poškození lysolecitinem, který vzniká působení fosfolipázy na fosfatidylcholin ve žluči.
- Bakteriální zánět, který je přítomen u 50 – 85 % pacientů s akutní cholecystitidou.
Nejčastěji jsou izolovány echerichie, klebsiely, streptokoky a klostridia.
Klinický obraz – začíná jako ataka biliárních bolestí, které se progresivně zhoršují. 60 – 70 % pacientů má zkušenost podobných předchozích obtíží, které spontánně ustoupily. Jak se obtíže zhoršují, bolest se rozšiřuje do celého pravého horního kvadrantu s možným šířením do pravé lopatky, mezilopatkové oblasti a pravého ramene. Postupně vzniká obraz peritoneálního břicha s bolestivostí při dýchání. Dochází k nauzee, zvracení a ztrátě hmotnosti s možností hypovolemie. Ikterus bývá až pozdním znamením a je způsoben zánětlivým otokem žlučovodů nebo extramurálním tlakem reaktivně zvětšených lymfatických uzlin. Časté jsou horečky i třesavky. Pravý horní kvadrant je palpačně citlivý. Tenzní, zvětšený žlučník je přítomen ve 25 – 50 % případů, Murphyho příznak (zhoršení bolestí při nádechu při palpaci v pravém horním kvadrantu) bývá pozitivní. Pozdním příznakem je lokalizovaná tuhost břicha nad žlučníkem nebo oslabení peristaltiky při paralytickém ileu. Pokud nedojde k perforaci stěny žlučníku, je difuzní peritonitida vzácná.
Diagnostika – diagnóza je stanovena na základě anamnézy a fyzikálního vyšetření.
Typická je triáda: bolestivost pravého horního kvadrantu + horečka + leukocytóza.
Leukocytóza je obvykle v rozmezí 10 – 15 · 109/l s posunem doleva. U necelých 50 % pacientů je lehce zvýšený bilirubin (< 85 μmol/l) a 25 % pacientů i aminotransferázy (< 5x norma).
Ultrasonografie – konkrementy lze nalézt v 90 – 95 % případů, dále zesílení stěny žlučníku, tekutinu v okolí žlučníku a dilataci žlučovodů.
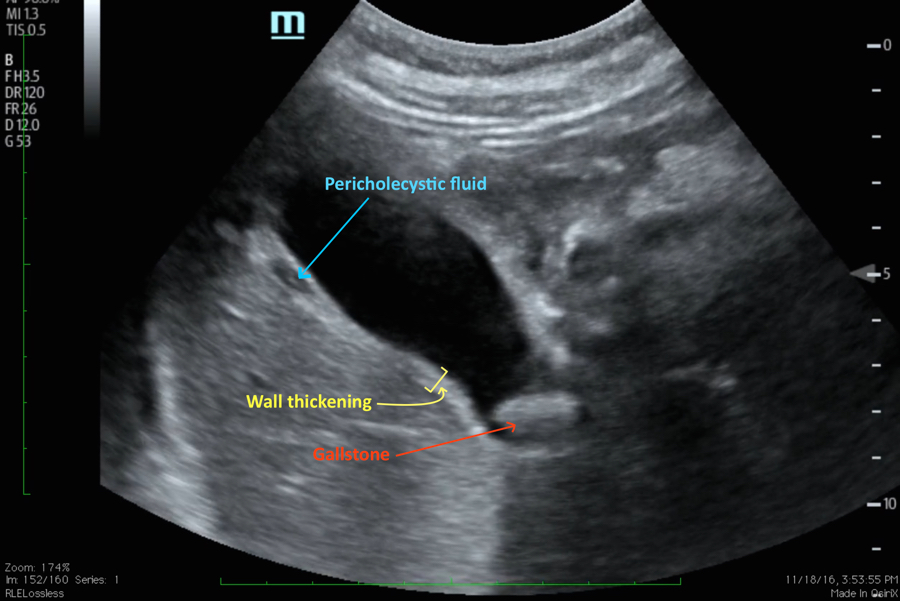
Radioizotopové metody – při HIDA se zobrazují žlučové cest, ale už ne žlučovod, což potvrzuje diagnózu.
Terapie – u cca 75 % pacientů dojde po 2 -7 dnech od začátku léčby k ústupu akutních obtíží, u 25 % i se i přes tuto léčbu stav komplikace s nutností chirurgické intervence
Režimová opatření – před cholecystektomií je nutná stabilizace pacienta (korekce hypovolémie a iontových poruch), eliminace perorálního příjmu, někdy je potřeba i zavedení nasogastrické sondy. K analgetizaci jsou vhodnější NSAID (ideálně se spasmolytickým efektem) než opioidy (zvýšení tonu Oddiho svěrače).
Antibiotika – při časné aplikaci antibiotik je i snížené riziko komplikací. Měla by být cílena proti nejčastějším původcům (E.coli, Klebsiella spp., Streptococcus sp.).:
- ureidopeniciliny (piperacilin, mezlocilin)
- aminopeniciliny (ampicilin-sulbaktam)
- fluorochinolony (ciprofloxacin, moxifloxacin)
- cefalosporiny 3. generace
Při podezření na:
- anaerobní infekci by měl být přidán metronidazol
- ascendentní cholangitidu by měl být přidán meropenem/imipenem, které mají být rezervovány na nejtěžší případy
Chirurgická terapie – pokud nejde o vitální indikaci je před chirurgickým výkonem vhodné pacienta stabilizovat. Zlatým standardem je provedení laparoskopické cholecystektomie do 24 hodin od přijetí. Oproti odloženému výkonu bylo sice zjištěna častější nutnost konverze v otevřený výkon, ale zároveň výrazně nižší četnost pooperačních komplikací (doi: 10.33699/PIS.2019.98.12.492–496).
Urgentní cholecystektomie nebo cholecystostomie je indikovaná u pacientů s podezřením na empyém, emfyzematózní cholecystitidu nebo perforaci. U pacientů ve vážném stavu je často vhodnější provedení cholecystostomie s drenáží žlučníku s provedením cholecystektomie v druhé době po zlepšení stavu.
Prognóza – po konzervativně zaléčené epizodě akutní cholecystitidy dojde k jejímu relapsu u 25 % pacientů do 1 roku a u 60 % pacientů do 6 let. S ohledem na dlouhodobou prognózu je nejlepší volbou provedení elektivní cholecystektomie, tak brzy jak je to jen možné.
Mortalita urgentní cholecystektomie je 3 %, u elektivní cholecystektomie je 0,5 % (u pacientů do 60 let).
Akalkulózní cholecystitida
U 5 – 10 % pacientů s akutní cholecystitidou, kdy perioperačně není nalezena obstrukce ductus cysticus. Častěji se vyskytuje u jiných systémových chorob (sarkoidóza, kardiovaskulární choroby, tuberkulóza, syfilis, aktinomykóza atd.). Rizikovým faktorem je diabetes mellitus.
Etiologie – typicky postihuje vážněji nemocné pacienty (to se podílí i na vážnější prognóze). Příčiny:
- ve > 50 % není nalezeno jiné vysvětlení probíhajícího zánětu, častější je sludge v ductus cysticus.
- více v pooperační periodě u závažných traumat, operačních výkonů, popálenin, protrahovaných porodů.
- při prolongované parenterální hyperalimentaci.
- při vaskulitidě.
- obturující adenokarcinom žlučníku.
- torze žlučníku.
- častější jsou neobvyklí původci cholcystitidy (Leptospira, Streptococcus, Salmonella, Vibrio cholerrae, parazité).
Klinický obraz – průběh je často mírný nebo mitigovaný základní chorobou, pokud jsou příznaky přítomny, odpovídají akutní cholcystitidě jiné etiologie. Typická je souběžnost s jinou závažnou komorbiditou.
Diagnostika – ultrazvuk, CT a radionuklidové metody zobrazí zvětšený, napjatý žlučník bez konkrementů se zhoršenou motilitou. Komplikace mohou být stejné jako u kalkulózní cholecystitidy.
Terapie – brzká diagnóza a cholecystektomie.
Akalkulózní cholecystopatie
Postižení motility žlučníku se může projevit opakovanou biliární bolestí bez průkazu litiázy. Ultrazvukově lze prokázat zvětšený žlučník. Infuzí cholecystokininu při cholescintigrafii lze měřit ejekční frakci žlučníku s nálezem jejího snížení typicky na < 40 %. Při chirurgické revizi se mohou prokázat různé abnormality jako chronická cholecystitida, hypertrofie svaloviny žlučníku nebo zúžený ductus cysticus. U části nemocných je v anamnéze předchozí onemocnění žlučníku. Podobnými obtížemi se manifestuje i stenóza Oddiho svěrače. Kritéria:
- Recidivující bolesti pravého horního podžebří.
- Abnormální radionuklidová cholecystografie s cholecystokininem s ejekční frakcí žlučníku < 40 %.
- Infuze cholecystokininu vyvolá typickou bolest.
Emfyzematózní cholecystitida
Při klasické kalkulózní nebo akalkulózní cholecystitidě může dojít k ischemii nebo gangréně, kterou mohou kolonizovat bakterie produkující plyn. Nejvíce ohroženi jsou starší muži a diabetici. Nejčastějšími původci z anaerobů jsou Clostridium welchii a perfringens, z aerobů E. coli. Klinický obraz je neodlišitelný od ostatních cholecystitid. Průkazný je nativní RTG břicha, ideálně CT břicha, na kterém lze nalézt prstenec plynu v okolí žlučníku nebo pericholecystické tkáně. Nutná je rychlá chirurgická intervence v kombinaci s antibiotiky. Stav má vysokou mortalitu.
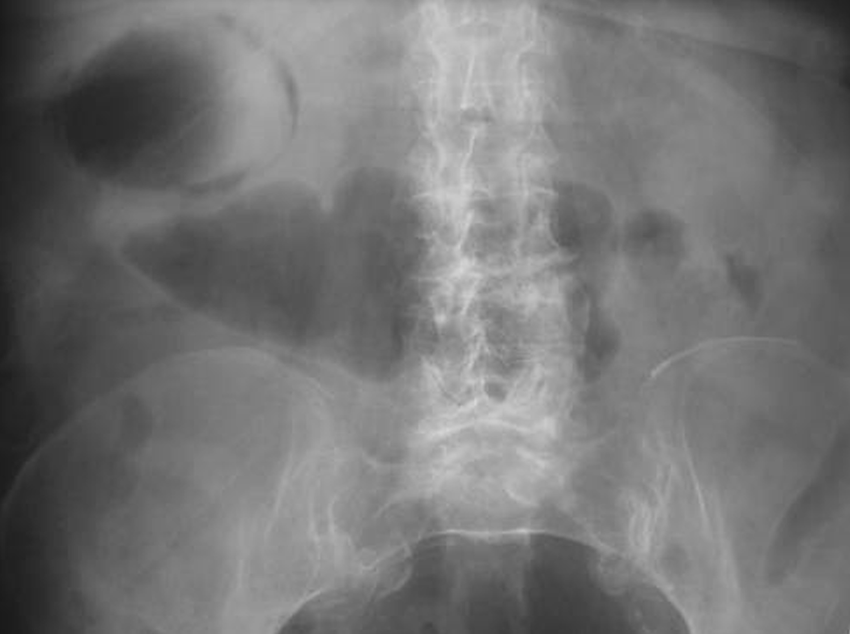
Chronická cholecystitida
Je téměř vždy spojena s přítomností cholecystolitiázy a vzniká:
- opakovanými reparacemi žlučníku po recidivujících záchvatech akutní cholecystitidy.
- dlouhodobou mechanickou iritací stěny žlučníku cholecystolitiázou.
U > 25 % je pozitivní kultivace žluči na baktérie, což zvyšuje riziko při cholecystektomii. Může být dlouhé roky asymptomatická, může exacerbovat do akutní cholecystitidy nebo se projevit komplikacemi (viz níže).
Komplikace cholecystitidy
Empyém – vzniká progresí akutní cholecystitidy s perzistující obstrukcí ductus cysticus se superinfekcí stagnující žluče pyogenními organismy. Klinicky jsou přítomné vysoké horečky, těžké bolesti pravého horního kvadrantu, výrazná leukocytóza a celkové zhoršení stavu. Často progreduje do G- sepse nebo dochází k perforaci žlučníku. Léčbou je emergentní chirurgická intervence s krytím antibiotiky.
Hydrops – vzniká také z protrahované obstrukce ductus cysticus, většinou velkým solitárním konkrementem. Zvýšeným tlakem dochází postupně k distenzi žlučníku s jeho naplněním hlenem (mucocele) nebo transudátem (hydrops), které jsou produkovány mukózními epiteliálními buňkami. Klinicky je přítomen viditelný, lehce palpovatelný, žlučník v pravém horním kvadrantu (někdy se šířící až do pravé ilické fossy). Pacient často zůstává asymptomatický nebo trpí chronickými bolestmi pravého horního kvadrantu. Léčebným postupem volby je cholecystektomie, protože je zvýšené riziko empyemu, perforace nebo gangrény.
Gangréna – gangréna žlučníku vzniká z ischemizace stěny s její částečnou nebo kompletní nekrózou. Na pozadí může být přítomen hydrops, vaskulitida, empyém nebo torze (arteriální okluze). Riziko je zvýšené u diabetiků. Gangréna může progredovat do perforace žlučníku.
Perforace – vzniká následkem gangrény nebo chronické cholecystitidy. Klasifikace:
- Lokalizovaná perforace – často ohraničena omentem nebo adhezemi, které vznikly při předchozích atakách cholecystitidy. Bakteriální superinfekcí může vzniknout absces. Léčebným postupem volby je cholecystektomie, u pacientů ve vážném stavu může být provedena cholecystostomie a drenáž abscesu.
- Volná perforace – méně častá, je charakterizována náhlým zmírněním bolestí (perforace a dekomprese sníží napětí stěny žlučníku) s následným rozvojem peritonitidy. Mortalita je cca 30 %.
Vznik píštěle – píštěle pronikají do okolních orgánů v následujícím pořadí: hepatální flexura kolon > žaludek nebo jejunum > břišní stěna > ledvinná pánvička. Klinicky němé cholecysto-enterické píštěle (jako následek předchozí cholecystitidy) byly nalezeny u více než 5 % pacientů, u kterých byla provedena cholecystektomie. Mohou být náhodně prokázány nálezem plynu v biliárním stromu při prostém snímku břicha. K jejich verifikaci lze použít RTG kontrastní vyšetření za použití barya. Léčba u symptomatických pacientů zahrnuje cholecystektomii, revizi ductus choledochus a uzávěr píštěle.
Biliární ileus – vzniká pasáží velkého žlučového konkrementu do lumen střeva (většinou přes cholecysto-enterickou píštěl) s následnou mechanickou obstrukcí. Místem obstrukce je většinou ileocékální chlopeň (za předpokladu, že proximálněji není striktura tenkého střeva). Anamnestický údaj o předchozích biliárních obtížích u většiny pacientů chybí. Velké konkrementy (> 2,5 cm) působí mechanickou erozi fundu žlučníku s následným možným vznikem píštěle, přes kterou se dostane konkrement do lumina střeva a vznikem ileu. Na nativním RTG břicha je diagnostická Riglerova triáda: 1. Ileus (hladinky), 2. Pneumobilie (plyn v biliárním stromu prokazuje nepřímo píštěl), 3. Ektopicky uložený, kalcifikovaný konkrement. Je indikována laparotomie s extrakcí konkrementu nebo jeho vypuzením do tlustého střeva.
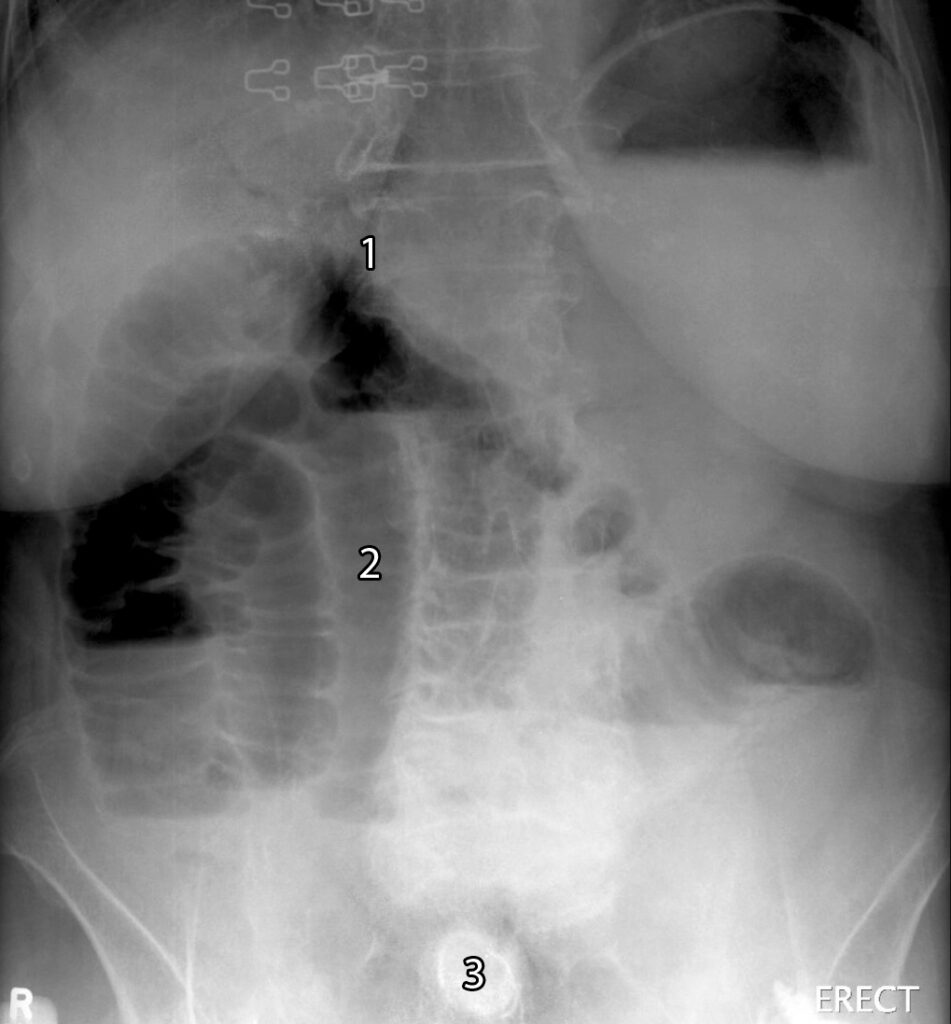
Vápenitá žluč – pokud dosáhnou kalciové soli v lumen žlučníku určité koncentrace, mohou precipitovat se vznikem difuzně bíle zakalené žluči. Tento nález je klinicky nevýznamný, přesto je indikována cholecystektomie, zejména pokud se vyskytne v terénu hydropického žlučníku.
Porcelánový žlučník – depozita kalcia ve stěně, chronicky zánětlivě změněného žlučníku mohou být detekována na nativním RTG vyšetření břicha. Vždy je indikována cholecystektomie, protože je zvýšené riziko progrese do karcinomu žlučníku.
Komplikace po cholecystektomii
- společné všem operačních výkonech – ARDS, atelektázy, vznik abscesu, krvácení.
- biliární – biliárně-enterická píštěl, žlučový leak. Ikterus z důvodu žlučového leaku se vznikem kolekce intraabdominálně s následnou resorpcí bilirubinu a dále mechanickou obstrukcí ductus choledochus (retinovaný konkrement, intraduktální krvavé zátky nebo komprese zvenku).
- specifické:
- cystic duct stump syndrome – recidiva biliárních bolestí u pacientů po cholecystektomii bez průkazu cholodocholitiázy byla původně přičítána příliš dlouhému (> 1 cm) pahýlu ductus cysticus, nyní se ale tato příčina zpochybňuje.
- papilární stenóza – může být způsobena akutním nebo chronickým zánětem Vaterské papily nebo glandulární hyperplazií papilárního segmentu. Pokud je ERCP neproveditelné, je jeho alternativou MRCP. Kvantitativní hepatobiliární scintigrafie prokazuje prodloužený průchod látky z ductus choledochus do střevního lumina, dilataci ductus choledochus a abnormální aktivitu v reálném čase. Toto je vhodné provést před a po papilisfinkterotomií k průkazu zlepšení biliárního vyprazdňování. Léčbou volby je endoskopická nebo chirurgická sfinkteroplastika k zajištění dostatečné drenáže jak ductus choledochus, tak ductus pancreaticus. Kritéria:
- 1) Bolesti břicha, většinou pravého horního kvadrantu nebo epigastria.
- 2) Abnormální jaterní testy.
- 3) Dilatace ductus choledochus při ERCP.
- 4) Prodloužená (> 45 minut) drenáž kontrastní látky z duktu.
- 5) Zvýšený klidový tonus Oddiho svěrače.
- dyskineze Oddiho svěrače – dochází ke spazmům svěrače, příčinou může být denervace vedoucí k hypertonu a vzniku abnormálních kontrakčních vln Oddiho svěrače. Diagnóza se určuje per exclusionem, sugestivní je nález abnormální ERCP a sfinkterové manometrie. Vhodnou léčbou je podávání nitrátů a anticholinergik ke zvýšení relaxace svěrače. Při neúspěchu po dvouměsíční farmakologické léčbě, je indikována EBS (endoskopická biliární sfinkterotomie ) nebo chirurgická sfinkteroplastika. EBS je léčbou volby při současné nutnosti extrakce konkrementu.
- gastritida a průjem indukovaný žlučovými solemi – u pacientů po cholecystektomii dochází často k rozvoji dyspepsie, která může být způsobena duodenogastrickým refluxem žluče. Po cholecystektomii vznikají trvalé změny v motilitě střeva. Cholecystektomie zkracuje průchod stolice střevem, zejména v pravé části colon, což způsobuje zvýšený výdej žlučových kyselin a posun k více projímavým sekundárním žlučovým kyselinám. Průjem je často úporný (> 3 vodnaté stolice denně) a objevuje se u 5 – 10 % pacientů po cholecystektomii. Léčebným pokusem může být podání látek, které váží žlučové kyseliny (cholestyramin, colestipol).
Hyperplastické cholecystózy
Skupina chorob, která je charakteristická excesivní proliferací normálně se vyskytujících tkání žlučníku.
Adenomyomatóza – benigní proliferace epitelu žlučníku se žlázovými formacemi, příčnými strikturami a adenomatózními nebo adenomyomatózními změnami fundu.
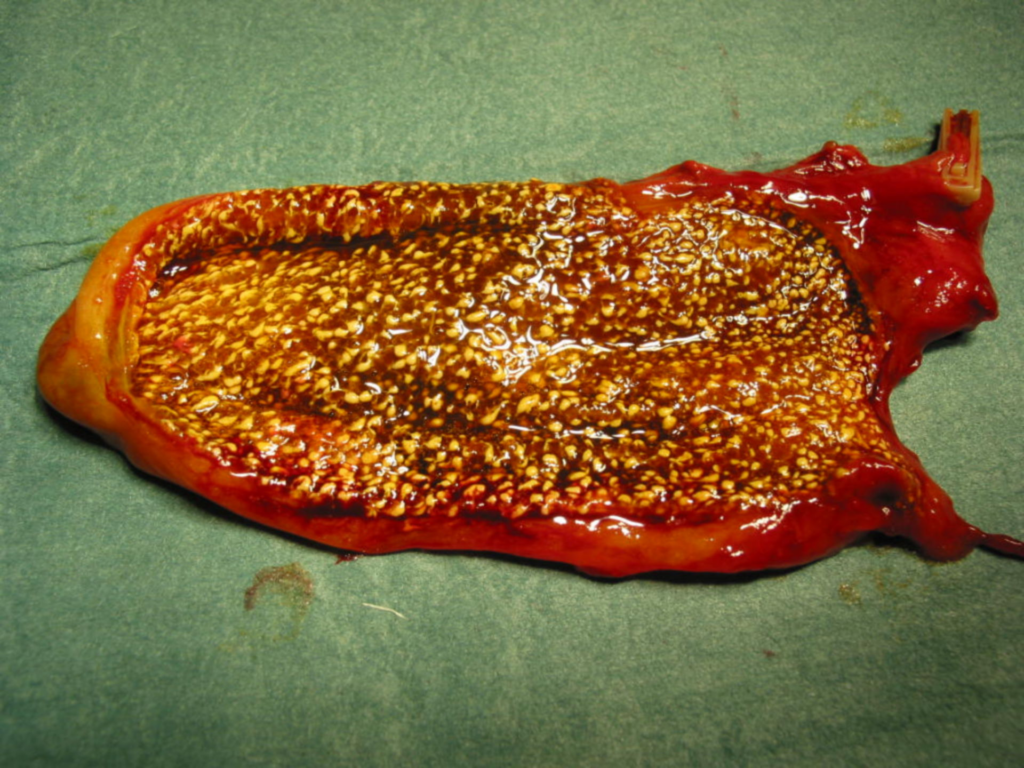
Cholesterolosis – abnormální depozice lipidů, zejména esterů cholesterolu v makrofázích v lamina propria stěny žlučníku. V téměř 50 % je přítomna i cholecystolitiáza. Při difuzní formě („jahodový žlučník“) je sliznice žlučníku tmavě červená se žlutými tečkovitými depozity lipidů. Při lokalizované formě jsou přítomny solitární nebo mnohočetné cholesterolové polypy stěny žlučníku. Jak při adenomyomatóze, tak cholesterolóze je indikována cholecystektomie pokud jsou přítomny klinické obtíže nebo cholecystolitiáza.
Polypy žlučníku
Prevalence v dospělosti je cca 5 %, s výraznou převahou u mužů. Jedinou léčbou je cholecystektomie. Mezi její indikace patří:
- symptomatičtí pacienti.
- pacienti > 50 let.
- při asociaci s cholecystolitiázou.
- velikost polypu > 10 mm nebo zvětšující se polyp.
Choroby žlučových cest
Vrozené anomálie žlučových cest
Biliární atrézie a hypoplazie – atrézie a hypoplazie extrahepatálních a velkých intrahepatálních žlučovodů jsou nejčastějšími vrozenými poruchami žlučových cest. Projevuje se těžkým obstrukčním ikterem se světlou stolicí, které se objevují v prvním měsíci života. Při podezření se provádí potvrzení chirurgicky a perioperační cholangiografií.
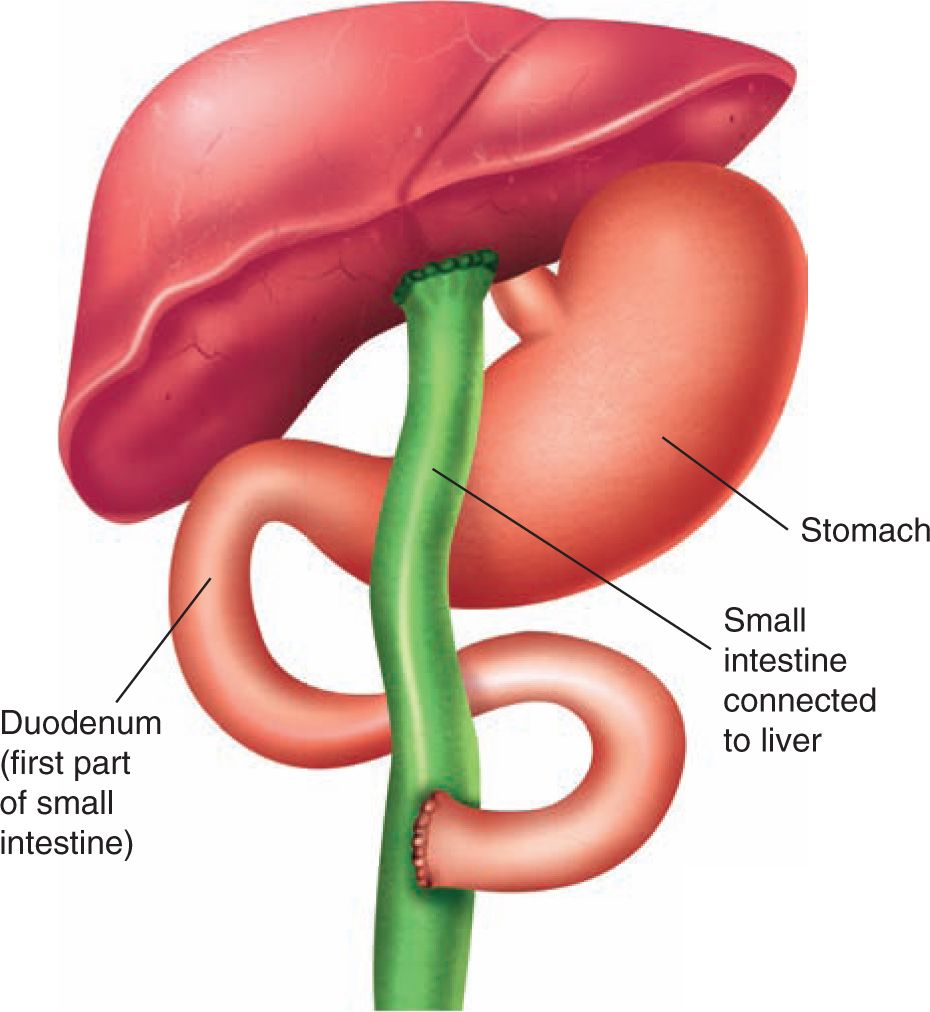
10 % případů biliární atrézie je léčitelných roux-en-Y choledochojejunostomií s výkonem dle Kasaie (jaterní porto-enterostomie). U většiny pacientů (i přes úspěšnou enterostomii) se nakonec vyvine chronická cholangitida a jaterní cirhóza s portální hypertenzí.
Cysty ductus choledochus – mohou být přítomny ve volné části ductus choledochus nebo prominovat jako divertikulární formace v intraduodenálním segmentu. V pozdních stádiích působí chronický reflux pankreatických šťáv do biliárního stromu a zánět s následnou stenózou extrahepatických žlučovodů, což vede k cholangitidě s biliární obstrukci. Proces progreduje a u 50 % pacientů dochází ke vzniku příznaků ve věku 10 let. Pouze u 1/3 pacientů se projevuje klasická trias příznaků: abdominální bolestivost + hmatná rezistence + ikterus. Je zvýšené riziko cholangiokarcinomu. Ultrazvuk, CT, MRI nebo cholangiografie prokazují cysty bez souvislosti se žlučníkem, které komunikují s ductus choledochus. Léčbou je excize cyst s biliárně-enterickou anastomózou.
Kongenitální biliární ektázie – dilatace intrahepatických žlučovodů může postihnout:
- hlavní nitrojaterní kmeny (Caroliho choroba).
- inter a intralobulární žlučovody (kongenitální hepatální fibróza).
- nebo žlučovody obou kalibrů.
Caroliho choroba – manifestuje se rekurentní cholangitidou s abscesovými formacemi a častou litiázou uvnitř dilatovaných žlučovodů. Ultrazvuk, CT nebo MRCP prokážou cystické dilatace. Léčebně i profylakticky se podávají antibiotika k omezení četnosti cholangitid, stav je často komplikován progresí do sekundární biliární cirhózy s portální hypertenzí, biliární obstrukcí, cholangiokarcinomem nebo rekurentními sepsemi a jaterními abscesy.
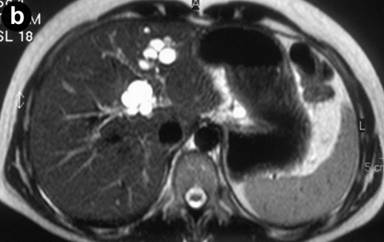
Choledocholitiáza
Patofyziologie – průchod žlučového kamene ze žlučníku do ductus choledochus provází 10 – 15 % případů cholecystolitiázy. Toto riziko stoupá s věkem, ve skupině starších pacientů se choledocholitiáza objevuje v čase cholecystektomie u > 25 % pacientů, přičemž u 1 – 5 % pacientů zůstává konkrement při cholecystektomii nepovšimnut. Na choledocholitiázu je nutné pomyslet u všech pacientů s cholecystolitiázou, kteří mají:
- anamnézu ikteru nebo pankreatitidy.
- abnormální jaterní testy.
- průkaz dilatovaného ductus choledochus nebo přímo konkrementů.
Většina vycestovaných konkrementů ze žlučníku je cholesterolových, zatímco většina de novo vzniklých konkrementů je pigmentových, které vznikají u pacientů s:
- parazity v hepatobiliárním stromu.
- rekurentními cholangitidami.
- Caroliho chorobou a jinými vrozenými a získanými anomáliemi hepatobiliárního stromu s dilatovanými a fibrotizovanými žlučovody.
- defektu genu MDR3, což vede ke snížení biliární sekrece fosfolipidů.
Choledocholitiáza může být asymptomatická po dobu mnoha let, může spontánně odejít do střeva, ale nejčastěji působí biliární koliku s komplikacemi:
Komplikace
1. Cholangitida – příznaky jsou výsledkem zánětu, který působí částečnou obstrukci toku žluči. U 75 % pacientů s akutní cholangitidou jsou ve žluči přítomny bakterie.
Přítomno Charcotovo trias: biliární bolest + ikterus + horečky s třesavkou.
Typická je leukocytóza a často i pozitivní hemokultura. Dělí se na formy:
- nesupurativní – nejčastější, dobrá odpověď na antibiotika.
- supurativní – hnisavá sekrece kompletně obturuje žlučovody s následným projevem těžké toxicity (mentální deteriorace, bakteriémie a septický šok), časté jsou mnohočetné abscesy jater. Antibiotika sama o sobě jsou neúčinná, je nutné rychlé odstranění obstrukce a zajištění drenáže endoskopicky nebo chirurgicky (bez těchto opatření je mortalita téměř 100 %). Jelikož je bezpečnější endoskopická intervence stejně účinná jako chirurgická je v současnosti preferována ERCP s papilosfinkterotomií.
2. Obstrukční ikterus – obstrukce ductus choledochus trvající týdny až měsíce vede ke vzniku ikteru s pruritem bez přítomnosti příznaku biliární koliky nebo cholangitidy. Je přítomen nárůst tlaku a dilatace intrahepatických žlučovodů s následným postižením toku žluče a porušením enterohepatického oběhu žlučových kyselin, což vede k posthepatálnímu ikteru (bilirubinurie s tmavou močí a světlá acholická stolice). Příčiny:
- choledocholitiáza – často se projevuje kolikou, vzácně bezbolestným ikterem. Velmi často přítomna i chronická kalkulózní cholecystitida.
- tumor hlavy pankreatu, žlučovodů nebo Vaterské papily.
Zvětšený, nebolestivý žlučník + ikterus se nazývá Courvoiserovob znamení (nevyskytuje je při choledocholitiáze a je vždy špatným znamením).
Podezření na choledocholitiázu by mělo vzniknout u každého pacienta s cholecystitidou, u kterého bilirubin převýší hladinu 80 μmol/l, ale jen zřídka dosáhne hladiny > 260 μmol/l (za předpokladu, že v pozadí není jiná hepatopatie, vždy je ale nutné vyloučit i extramurální útlak tumorem). Vždy je zvýšené ALP. ALT a AST bývají zvýšené 2 – 10x oproti normě, zejména pokud jde o akutní obstrukci. Po vyřešení obstrukce se ALT a AST rychle vrací k normálu, sérový bilirubin klesá pomaleji (cca 1 – 2 týdny), poslední se normalizuje ALP (ALT, AST → bilirubin → ALP).
3. Pankreatitida – choroba biliárního traktu je nejčastější příčinou nealkoholické akutní pankreatitidy. Biochemické známky iritace pankreatu jsou přítomny u 15 % akutní cholecystitidy a 30 % choledocholitiázy. Odstranění konkrementu v ductus choledochus vede většinou k vymizení pankreatitidy. Podezření by mělo vzniknout u každého pacienta s choledocholitiázou, u kterého je:
- bolestivost zad nebo levé části břicha.
- prolongované zvracení a paralytický ileus.
- pleurální iritace, zejména na levé straně bránice.
Sekundární biliární cirhóza
Může být komplikací dlouhodobé obstrukce ductus choledochus konkrementem. Mnohem častější příčinou obstrukce bývá striktura nebo útlak tumorem. Pokud je cirhóza pokročilá, může progredovat i po odstranění obstrukce. Při dlouhodobé biliární obstrukce může nastat klinicky zjevný deficit vitamínů rozpustných v tucích (A, D, E a K).
Diagnostika
| Výhody metody | Limitace metody | Kontraindikace | Komplikace | Poznámky |
| Ultrazvuk břicha | ||||
| rychlost | plyn ve střevě | nejsou | nejsou | metoda prvního kontaktu |
| vyšetření ostatních struktur břicha | masivní obezita | |||
| přesná identifikace dilatovaných žlučovodů | ascites | |||
| není omezení ikterem ani těhotenstvím | baryum | |||
| navigace pro biopsii | částečná biliární obstrukce | |||
| špatná vizualizace distálních žlučovodů | ||||
| CT | ||||
| vyšetření ostatních struktur břicha | extrémní kachexie | těhotenství | reakce na jodovou kontrastní látku | vhodné k zobrazení tumorů jater nebo pankreatu |
| přesná identifikace dilatovaných žlučovodů a expanzí | pohybové artefakty | metoda prvního kontaktu, při limitacích ultrazvuku břicha | ||
| není limitace ikterem, střevním plynem, obezitou a ascitem | ileus | |||
| vysoká rozlišovací schopnost | částečná biliární obstrukce | |||
| navigace pro biopsii | ||||
| MRCP | ||||
| přesná vizualizace pankreatických vývodů a žlučovodů | vysoká cena | klaustrofóbie | nejsou | |
| nejsenzitivnější pro dilataci žlučovodů, biliárních striktur a intraduktálních abnormalit | nelze v jedné době terapeuticky zasáhnout | kov v organismu | ||
| identifikace dilatace, striktury a stenózy pankreatických vývodů, identifikace pancreas divisum | ||||
| ERCP | ||||
| simultánní pankreatografie | obstrukce gastroduodena | těhotenství | akutní pankreatitida, | metoda volby při: |
| nejlepší identifikace distálních žlučovodů | Roux – Y biliárně – enterická anastomóza | akutní pankreatitida | cholangitida, sepse | absenci dilatovaných žlučovodů |
| odběr vzorku žluče nebo pankreatické cytologie | těžká kardiopulmonální choroba | infekční pankreatická pseudocysta | plánované biliární chirurgii | |
| provedení papilosfinkterotomie | perforace | předpoklad provedení sfinkterotomie | ||
| biliární manometrie | hypoxie, aspirace | |||
| Perkutánní transhepatická cholangiografie | ||||
| extrémně úspěšná při dilatovaných žlučovodech | nedilatované nebo sklerotické žlučovody | těhotenství | krvácení | při kontraindikaci nebo selhání ERCP |
| nejlepší vizualizace proximálních žlučovodů | nekorigovaná koagulopatie | hemobilie | ||
| odběr vzorku žluče nebo cytologie | masivní ascites | biliární peritonitida | ||
| současné zavedení perkutánní transhepatické drenáže | jaterní absces | bakteriémie, sepse | ||
| Endoskopický ultrazvuk | ||||
| nejsenzitivnější metoda k detekci ampulární litiázy |
Diagnostika choledocholitiázy se potvrdí nejčastěji ERCP, MRCP nebo perioperačně při cholecystektomii (u 15 % pacientů se při cholecystektomii prokáže i choledocholitiáza). Pokud se choledocholitiáza prokáže ještě před operací je metodou volby ERCP s papilosfinkterotomií a extrakcí konkrementu a v druhé době se provede cholecystektomie (výhodou je jistota v odstranění konkrementu a také zmapování biliárního stromu ve vztahu k ductus cysticus). Jelikož je cholecystektomie široce dostupná, klesá počet choledocholitotomií s drenáží a celkově počet komplikací.
Traumata a striktury biliárního stromu
Největší počet benigních striktur vzniká iatrogenně po cholecystektomii (incidence 1:500 provedených cholecystektomií). Striktury se mohou projevit biliárním leakem nebo tvorbou abscesu bezprostředně po cholecystektomii nebo opožděně (i 2 a více roků) biliární obstrukcí nebo cholangitidou. Diagnóza se potvrdí PTC nebo ERCP. Periprocedurálně je vhodné provedení endoskopického brushingu (přesnější než cytologie žluči) k vyloučení maligní povahy striktury. Toto je důležité zejména u pacientů s primární biliární cirhózou, kteří jsou velice predisponováni ke vzniku cholangiokarcinomu. Léčbou striktury je chirurgická korekce biliárně – enterickou anastomózou (vysoká mortalita výkonu zejména díky chirurgickým komplikacím, rekurentní cholangitidě a sekundární biliární cirhóze).
Hemobilie
Etiologie – poranění jater nebo žlučovodů (trauma nebo jako chirurgická komplikace), komplikace choledocholitiázy, intraduktální ruptura, jaterní absces, aneurysma jaterní arterie, tumor jater nebo žlučovodů, hepatobiliární parazitismus, komplikace diagnostických metod (jaterní biopsie, PTC, umístění transhepatického drénu).
Klinický obraz – typické trias = biliární bolest + obstrukční ikterus + krvácení ve stolici nebo meléna.
Diagnostika – cholangiograficky lze prokázat krevní zátky v biliárním stromě, někdy je nutné zdroj nutné objasnit selektivní angiografií.
Terapie – minimální hemobilie může spontánně odeznět, často je ale potřeba chirurgické ošetření.
Vnější komprese žlučovodů
Nejčastěji karcinom hlavy pankreatu, akutní nebo chronická pankreatitida, postižení lymfatických uzlin porty hepatis lymfomem nebo metastatických karcinomem. Vnější komprese může způsobit částečnou nebo kompletní obstrukci žlučovodů. Toto musí být odlišeno od masivní infiltrace jater tumorem.
Hepatobiliární parazitismus
Etiologie
- v civilizovaných zemích vzácné, nejčastěji se vyskytuje v jižní Číně a Jihovýchodní Asii. Původcem jsou trematody a červy (Clonorchis sinensis, Opisthorchis viverrini, Opisthorchis felineus a Fasciola hepatica).
- postižení jater může být také způsobeno intraduktální migrací dospělých Ascaris lumbricoides z duodena
- nebo intrabiliární rupturou hydatidových cyst jater, které vytváří Echinococcus spp.
Klinický obraz – chronická pyogenní cholangitida s nebo bez mnohočetných abscesů, choledocholitiázou nebo biliární obstrukcí.
Diagnostika – cholangiografie + průkaz vajíček ve stolici.
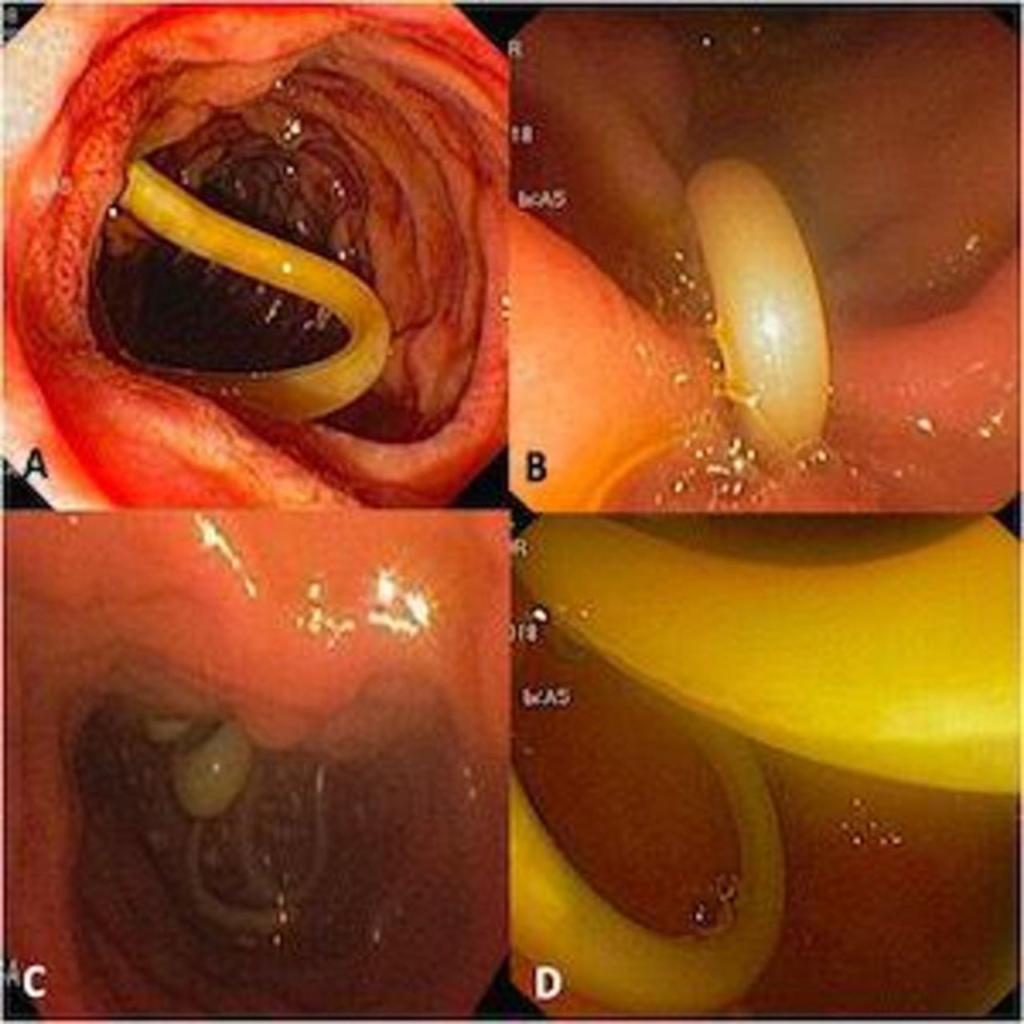
Terapie – při průkazu obstrukce je metodou volby laparotomie pod clonou antibiotik s drenáží ductus choledochus a biliárního stromu.
Sklerozující cholangitidy
Cholangitida asociovaná s imunoglobulinem G4 – choroba klinicky totožná s primární sklerozující cholangitidou a je často spojena s autoimunitní pankreatitidou. Jaterní tkáň a žlučovody jsou infiltrovány IgG4-pozitivními plazmocyty a v séru je zvýšené IgG4. Není ale spojena s ulcerózní kolitidou. Podezření by mělo vzniknout u pacientů se zvýšeným IgG4 a neobjasněnou poruchou pankreatu. Lékem volby jsou glukokortikoidy s detrakcí. Po jejich vysazení dochází často k relapsu s nutností dlouhodobé léčby kombinace glukokortikoidů a azathioprinu.
Cholangitida asociovaná s AIDS – cholangiopankreatografie prokazuje široké spektrum poškození žlučových cest (intra- i extrahepatických žlučovodů nebo ampulární poškození) a obstrukci ductus pancreaticus s event. pankreatitidou. U 10 % pacientů se vyskytuje akalkulózní cholecystitida. Úlevu často poskytne ERCP s papilosfinkterotomií.
Primární sklerozující cholangitida (PSC)
Charakterizována progresivní zánětlivou sklerózou a obliterací postihující extra- a/nebo intrahepatální žlučovody.
CAVE v 75 % je v asociaci s nespecifickým střevním zánětem (zejména ulcerózní kolitidou).
Může se dále asociovat s autoimunitní pankreatitidou, multifokální fibrosklerotickým syndromem (retroperitonea, nebo mediastina), periureterální fibrózou, Riedelovou strumou nebo pseudotumorem orbity.
Klinický obraz – projevuje se známkami chronické nebo intermitentní biliární obstrukce, bolestí pravého horního kvadrantu, pruritem, ikterem nebo akutní cholangitidou. V pozdních stádiích se objevuje sekundární biliární cirhóza se všemi komplikacemi. Nezávislými prediktory špatné prognózy jsou věk, vysoká hladina bilirubinu a pokročilé změny v jaterní biopsii.
Studie: Švédsko, 305 pacientů s primární sklerozující cholangitidou. 44 % (134) bylo v době stanovení asymptomatických s lepší prognózou. 8 % pacientů s nálezem cholangiokarcinomu. 81 % pacientů s prokázaným nespecifickým střevním zánětem.
Diagnostika – ERCP nebo MRCP – difuzní, multifokální striktury žlučovodů, které jsou střídány normálními nebo dilatovanými segmenty.
Při normální cholangiografii, přítomné chronické cholestáze a nálezu primární sklerozující cholangitidy v jaterní biopsii jde o dominantní postižení malých žlučovodů (small duct PSC). Vyskytuje se u 5 % případů primární sklerozující cholangitidy a jde pravděpodobně o časné stádium s následnou progresí a postižením i velkých žlučovodů.
CAVE při potvrzení choroby je nutno ihned vyloučit postižení střeva nespecifickým zánětem.
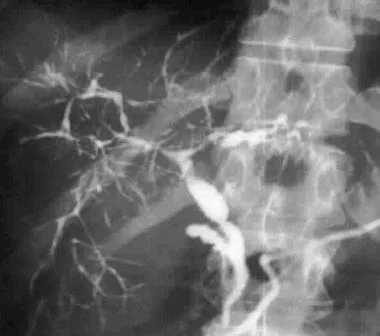
Terapie
- podpůrná léčba – cholestyramin při pruritu, antibiotika při akutní cholangitidě, kalcium a vitamín D jako prevence sekundární osteoporózy při dlouhodobé cholestáze
- kyselina ursodeoxycholová ve vysokých dávkách (20 mg/kg) zlepšuje jaterní testy, ale nezlepšuje prognózu. Glukokortikody, metotrexát a azathioprin jsou bez efektu.
- balónková dilatace – při těžké obstrukci se strikturami. Chirurgická intervence je indikována jen vzácně.
- transplantace jater – PSC je jedna z nejčastějších indikací k transplantaci jater.
Prognóza – nepříznivá s mediánem přežití 10 let od stanovení diagnózy. Riziko se stanovuje na základě čtyř proměnných: věk, sérový bilirubin, histologický nález, splenomegalie.
Ostatní cholangitidy
Sekundární sklerozující cholangitidy vznikají jako pozdní komplikace choledocholitiázy, cholangiokarcinomu, traumatu biliárního stromu nebo chronických zánětlivých procesů.