Leukocyty se fyziologicky vyskytují v množství 4 – 10 × 109/l:
- neutrofily 55 – 70 % (2,5 – 7 × 109/l, z toho tyčky 2 – 6 %)
- lymfocyty 25 – 40 %, (1,5 – 4 × 109/l)
- monocyty 2 – 8 % (0,2 – 0,9 × 109/l)
- eozinofily 1 – 4 % (0,05 – 0,5 × 109/l)
- bazofily 0 – 1 % (0 – 0,15 × 109/l)
Neutrofily
Neutrofily jsou pro produkovány pouze v kostní dřeni v obrovském množství (130 miliard denně). Zvýšení množstí neutrofilů se označije jako neutrofilie, zvýšená přítomnost nezralých forem jako posun doleva. Celkový vývoj neutrofilu trvá 14 dnů:
- myeloblast – první fáze, následuje
- promyelocyt – tvoří primární granula (obsahují hydrolázy, elastázy, myeloperoxidázu, kathepsin, kationický protein, defenziny atd.), poté
- myelocyt – tvoří sekundární granula (obsahují laktoferin, vitamín B12 vazebný protein, komponenty NADPH oxidázy), dále se již buňky nedělí, následuje
- metamyelocyt a poté
- zralý neutrofil tyčka – tyčkovité jádro dává vznik několika lalokům (cca 4 – 5), tzv.
- zralý neutrofil segmentární – ke vzniku > 5 laloků dochází např. při deficitu vitamínu B12 nebo kyseliny listové. Jako tzv. Pelger – Hüetova anomálie se označuje vzácná benigní situace s dvoulaločnatým jádrem.
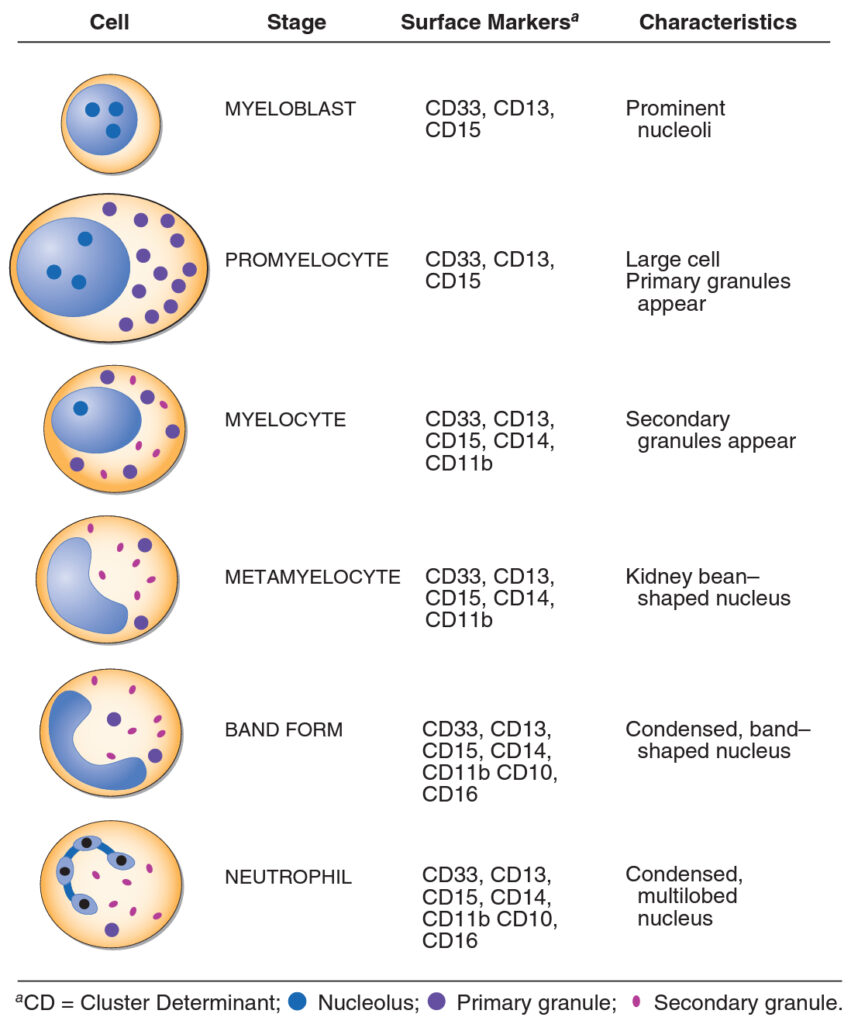
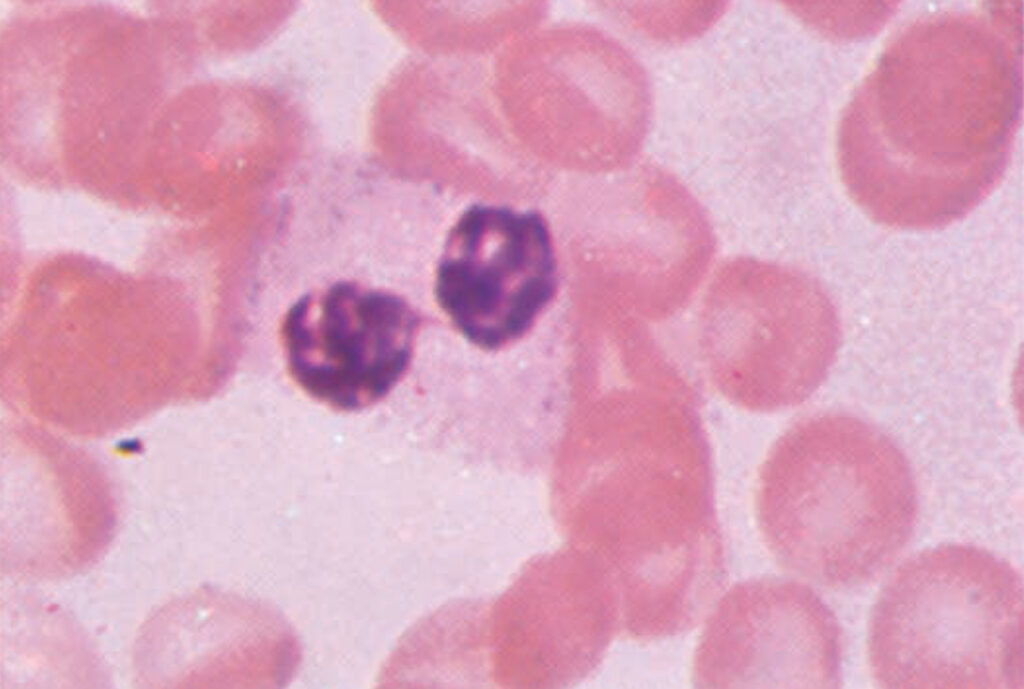
Při těžké bakteriální infekcí dochází ke vzniku četných cytoplazmatických neutrofilních granul označovaných jako toxické granulace. Při infekci lze nalézt i cytoplazmatické inkluze označované jako Döhleho tělíska (agregáty drsného endoplazmatického retikula). Z kostní dřeně jsou neutrofily rekrutovány pomocí zánětlivých elementů (IL-1, -6, TNF-alfa, fragmenty komplementu apod.).
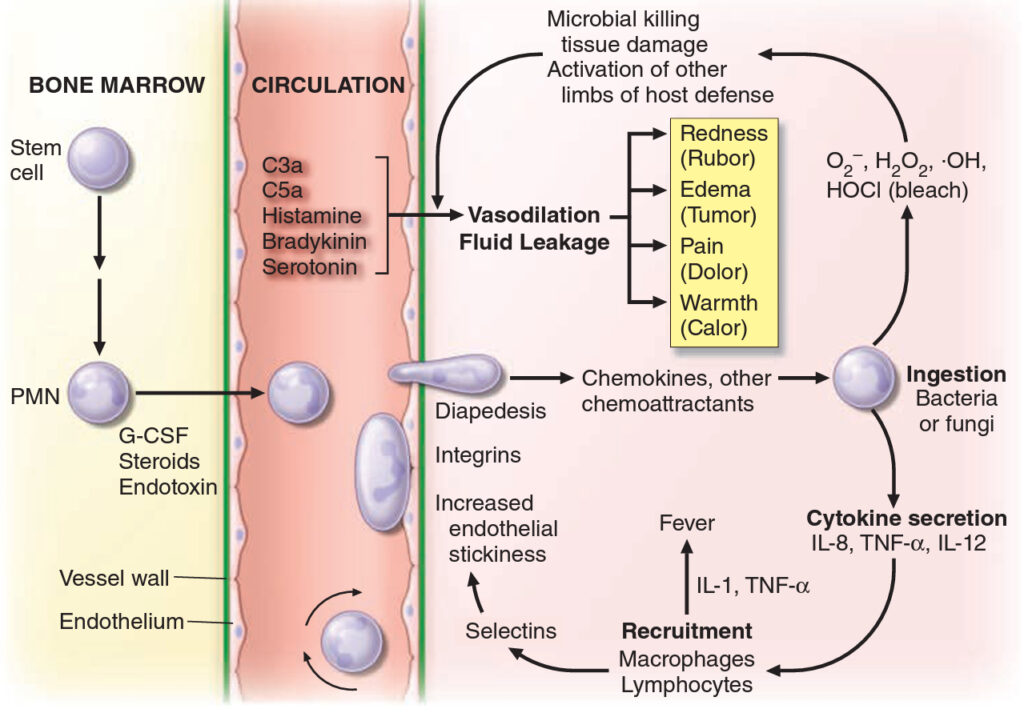
V kostní dřeni je deponováno cca 90 % všech neutrofilů, 2- 3 % poolu je v cirkulaci a zbytek ve tkáních. Cirkulující pool lze rozdělit na dva dynamické kompartmenty, volně cirkulující neutrofily a marginální neutrofily, které jsou vázány na endotelie (cca 50 % / 50 %). Při průchodu plicními kapilárami je nutné, aby byly neutrofily výrazně deformovatelné. Extravazace má nekolik fází:
- vazba na endotel je zprostředkována glykoproteiny selektiny, díky kterým se neutrofil zpomaluje koulením (rolling) po povrchu endotelií. Na neutrofilech se nachází L-selektin (CD62L), který se váže na glyCAM-1 (CD34) endotelií, dále glykoprotein neutrofilů Sialyl-Lewis protein (CD15s) se váže na E-selektin (CD62E) a P-selektin (CD62P) endotelií. Tuto adhezi zvyšuje přítomnost chemotaktických stimulů (IL-8, C5a komplementu, leukotrien B4 apod.), které mobilizují leukocytární adheziny i endotelilální integriny a exprimují je na povrchu buněk.
- Po zpomalení leukocytů dochází k vazbě LFA-1 (CD11s/CD18) a CR-3 (CD11b/CD18) neutrofilů na ICAM-1 a -2 (CD54/CD102) endotelií. Pomocí CD31 a diapedézy následně dochází k extravazaci.
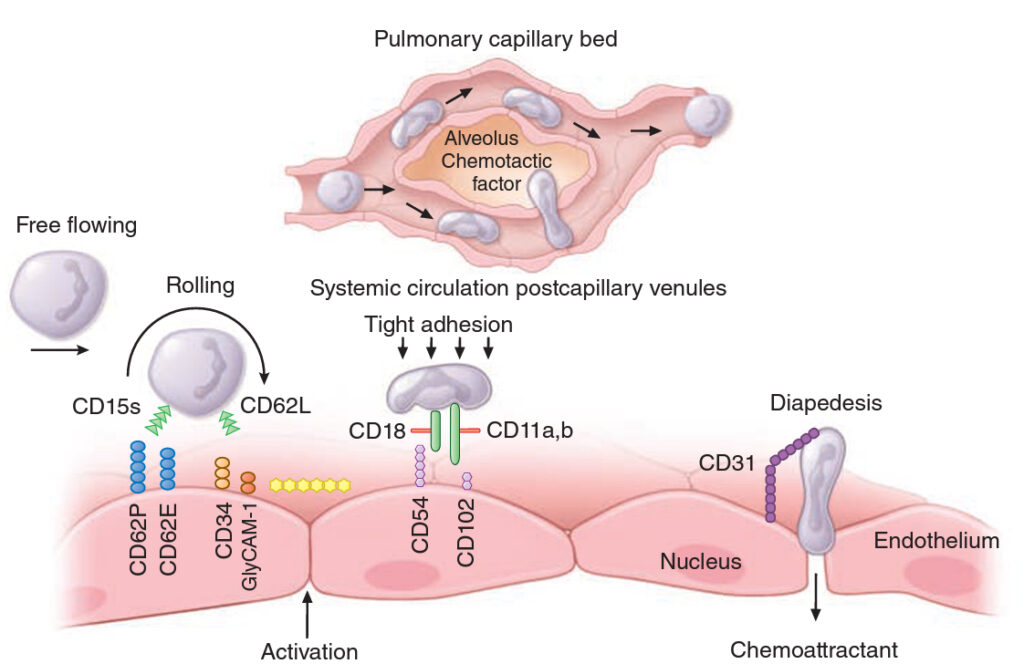
- Při infekci se zvyšuje množství neutrofilů ve tkáni a marginálním poolu (velké množství neutrofilů extravazuje).
- Při zvýšeném množství katecholaminu dochází k uvolnění neutrofilů do cirkulace a snížení marginace (tělo se připravuje na jejich potřebu).
- Po podání steroidů se uvolní neutrofily do krve (zvýšený je jak cirkulující, tak marginální pool…neutrofily jsou připraveny k extravazaci).
- Při LAD (leukocyte adhesion deficienci) by rády neutrofily extravazovaly, ale nemají jak (nízké množství na ve tkáních v marginální poolu).

V cirkulaci tráví neutrofily krátký čas (6- 7 hodin), velká část jich opouští tělo trávícím traktem, zbytek je odstraňován makrofágy v plicích a slezině. Pokud extravazují do tkáně, uvolňují kolagenázy a elastázy a fagocytují vše co je opsonizováno IgG a C3b. Po fagocytáze dochází k oxidačnímu vzplanutí se zvýšením aktivity NADPH oxidázy s produkcí superoxidového aniontu, který je následně konvertován pomocí superoxiddismutázy na H2O2 a hydroxylový radikál. Na likvidaci patogenů se podílí i další buněčné mechanismy. Neutrofily se výrazným způsobem podílí na tvorbě hnisu.
Porucha funkce neutrofilů vede k porušení zánětlivé reakce a zvýšení četnosti infekcí (kůže, ucha, horního a dolního respiračního traktu).
Neutropenie
K výrazně zvýšené predispozici k infekcím dochází při poklesu neutrofilů < 1 × 109/l, při < 0,2 již nedochází k lokální zánětlivé reakci. K neutropenii může dojít při snížení produkce a/nebo zvýšené destrukci a/nebo zvýšení marginálního poolu. Snížení produkce (léčbou je ovlivnění základního vyvolávajícího faktoru event. podání G-CSF) Příčiny:
- Léky působí útlum kostní dřeně (zejména imunosuprese/chemoterapie, ale někdy i např. Biseptol)
- Azathioprin – 11 % bílých jedinců má hypofunkční mutaci thiopurin methyltransferázy, která působí akumulaci azathioprinu a myelotoxicitu.
- Některé léky mohou působit jako hapteny (zejména peniciliny a cefalosporiny), taková neutropenie vzniká po cca týdnu prvoužívání léku, při znovunasazení léku do medikaci vzniká již po cca několika hodinách. Upravuje se po vysazení vyvolávajícího léku po cca 7 – 10 dnech.
- Cirkulující protilátky proto neutrofilům – např. při některých virových infekcích.
- Vrozené neutropenie – vzácné:
- Kostmannův syndrom – těžká vrozená neutropenie s počtem neutrofilů < 0,1 × 109/l.
- Cyklická neutropenie – AD dědičná či sporadická cyklicky se opakující porucha dělení kmenových buněk v kostní dřeni, manifestuje se nejčastěji po narozením. V intervalech cca 20 dní se objevuje neutropenie s horečkou a ulceracemi ústní sliznice, event. abscesy, osteomyelitidou a sepsí. Infekce se léčí antibiotiky, prognóza je dobrá.
- Těžká chronická neutropenie
- Schwachmann-Bodian-Diamondův syndrom – neutropenie + chronická pankreatická insuficience.
- Novorozenecká neutropenie – transplacentární přenos IgG prot nautrofilům od matky na plod. Neutropenii plodu moho způsobit i např. thiazidy.
- Feltyho syndrom – revmatoidní artritida + splenomegalie + neutropenie (slezina produkuje protilátky proti neutrofilům). Krajně může pomoci splenektomie.
Funkční poruchy neutrofilů viz http://mame-radi-internu.cz/jednotlive-obory-vnitrniho-lekarstvi/viii-imunologie/a112-imunodeficity/
Neutrofilie
Neutrofilie vzniká ze zvýšení produkce nebo uvolnění neutrofilů z kostní dřeně nebo defektu marginace. Mezi nejčastějí příčiny patří:
- zánět – infekce (zejména bakteriální a mykotické) ale i neinfekční (nekrózy, infarkty, popáleniny, kolagenózy apod.).
- léky – glukokortikoidy (zvýšení uvolnění z kostní dřeně a zvýšení marginace), G-CSF, adrenalin (snížení marginace)
- stres – viz adrenalin
- myeloproliferace
- ostatní
- akutní krvácení
- ketoacidóza
- LAD
Monocyty
Systém mononukleárů je složen z monoblastů, promonocytů, monocytů a tkáňově odlišných makrofágů (dohromady tvoří retikuloendoteliální systém). Monocyty mají poločas v cirkulaci 12 – 24 hodin, následně opouští krevní kompartment diapedézou a stávají se z nich makrofágy (zvýšené množství je přítomno v plicích, játrech, slezině a kostní dřeni, kd ese podílí na odstraňování mikrorganismů a ostatních nox (dle tkáně mají speciální označení: plíce – alveolární makrofágy, játra – Kupfferovy buňky, mozek – mikroglie apod.). Produkují lysozym, neutrální proteázy, kyselou hydrolázu, plazmin a řadu cytokinů (TNF-alfa, IL-1, -8, -12, -18).
IL-1 je pyrogen, mobilizuje leukocyty z kostní dřeně a aktivuje neutrofily a lymfocyty. TNF-alfa má některé vlastnosti podobné IL-1, navíc se spolupodílí na septickém šoku spojeném s G- infekcía kachexii chronických chorob.
Pomáhají regulovat replikaci lymfocytů a likvidovat nádorové buňky a buňky infikované viry a intracelulárními parazity. Dále mají schopnost splývat do obrovských buněk, které následně tvoří granulomy, což je pod kontrolou IFN-gama.
Jejich další důležitou vlastností je prezentace antigenu lymfocytům s následnou produkcí cytokinů modulujících jejich vývoj. Podílí se na odstranění imunokomplexů z cirkulace, vývoji aterosklerotického plátu a vzniku emfyzému uvolněním elastázy v alveolech.
Monocytóza – spojena s tuberkulózou, brucelózou, subakutní bakterkální endokarditidou, malárií a leishmaniázou, dále u malignit (solidních i hematologických nádorů) a granulomatózních chorob (např. sarkoidóza) apod.
Monocytopenie – u akutních infekcí, při stresu a léčbě glukokortikoidy a dále při všech stavech vedoucích k poškození kostní dřeně (např. aplastická anémie, myelotoxická terapie apod.).
Eozinofily
Silné složky obrany proti mnohobuněčným parazitům, které jsou regulovány pomocí IL-5 z antigen specifických Th2 lymfocytů (specifický imunitní systém reguluje nespecifický). Obsahují granula s hlavním bazickým proteinem, eozinofilním kationickým proteinem a neurotoxinem, které mohou přímo ničit okolní tkáň (hypereozinofilní syndrom).
Eozinofilie
Mezi nejběžnější příčiny eozinofilie patří:
- infekce mnohobuněčnými organismy (tasemnice, schistostomiáza, škrkavky, filarie, echinokok apod.)
- alergická reakce na
- léky (např. jód, ASA, betalaktamy apod.)
- jiné alergeny (pyl, seno apod.)
- alergické vaskulitidy, pneumonitidy apod.
- systémové choroby pojiva (revmatoidní artritida, eozinofilní granulomatóza s polyangitidou apod.)
- nádory
- hematologické (Hodgkinův lymfom, eozinofilní leukémie apod.)
- solidní (karcinom plic, žaludku, pankreatu, vajčníku, dělohy)
- idiopatický hypereozinofilní syndrom (Loefflerův syndrom)
- ostatní – Jobův syndrom
Idiopatický hypereozinofilní syndrom – skupina chorob s protrahovanou eozinofilií a orgánovou dysfunkcí (srdce, CNS, plíce, ledviny, GIT a kůže), která vzniká díky lokalizovanému působení toxických eozinofilních proteinů (např. eozinofilní kationický protein, hlavní bazický protein). V srdci dochází ke vzniku trombózy a endokardiální fibrózy. Terapeuticky lze použít glukokortikoidy, hydroxyureu, IFN-alfa a monmoklonální protilátky anti-IL5.
Eozinopenie – viz monocytopenie, bez klinického významu.