Definice – hypertrofická kardiomyopatie (HKMP) je definována jako zesílení stěny levé komory není vysvětlitelné hemodynamickými příčinami (nejčastěji přítomností arteriální hypertenze, chlopenní vady nebo vrozené srdeční vady…tedy podmíněná nejen hypertrofií kardiomyocytů, ale i intracelulární akumulací metabolických substrátů, např. amyloidóza, Fabryho choroba). Jako cut-off bývá považována tloušťka levé komory 15 a více mm (CAVE při geneticky a metabolicky potvrzených chorobách často stačí 13 mm).
Epidemiologie – prevalence 1:500.
Etiologie – nejčastější příčinou je familární (sarkomerická) forma, ostatní se označují jako nesarkomerické.
I. Sarkomerická HKMP
Definice – geneticky podmíněné onemocnění, které je způsobené mutací genů kódujících kontraktilní proteiny srdeční sarkomery. Většinou je přítomna AD dědičnost.
Etiologie– nejčastější je mutace genu těžkého řetězce β myozinu (MYH7, 40 %) a genu myozin vázajícího proteinu C (MYBPC3, 35 %), dále pro troponin T (4 %) a I (1‐2%) Určení typu mutace se povede pouze ve 35 – 60 % případů a typ mutace nevypovídá nic o další prognóze pacienta. Smyslem genetického testování je hlavně určení přítomnosti mutace a nutnosti dalšího došetření u příbuzných pacienta.
Příčinou vzniku hypertrofie je pravděpodobně kompenzace nesprávné funkce mutací postižené sarkomery. Většina pacientů má asymetrické rozložení hypertrofie (nejčastěji mezikomorové septum, méně často boční a dolní stěnu, v Japonsku je častější izolované postižení hrotu), u 30 % bývá hypertrofií postižena i pravá komora, často bývá abnormální i mitrální chlopeň s elongací jednoho nebo obou cípů nebo jinými změnami. Běžná je rozsáhlá fibróza myokardu.
Typickým mikroskopickým nálezem je myocardial disarray (dezorganizace myokardu se ztrátou paralelního uspořádání, četná fibróza, abnormální mezibuněčné spojení, tvar i velikost jednotlivých buněk), dochází ke zmenšení malých koronárních artérií se zúžením jeho lumen. Tímto nálezem je postiženo pouze 5 – 40 % veškerého myokardu, což sarkomerickou HKMP odlišuje od hypertrofií jiného původu.
Patofyziologie – pacienti s HKMP mají typicky malou dutinu levé komory s nadprůměrnou ejekční frakcí.
- LVOTO – 1/3 pacientů má klidový tlakový gradient mezi LVOT a aortou, u další 1/3 je tento gradient latentní (pouze při snížení preload a afterload předtížení nebo zvýšení kontraktility), který vzniká díky obstrukci LVOT (hypertrofická obstrukční KMP, HOKMP)Tato obstrukce bývá nejčastěji lokalizována v subaortální oblasti a téměř vždy je spojena se SAM (systolic anterior movement) předního cípu mitrální chlopně. Velké zrychlení toku krve při hypertrofii septa pravděpodobně nasaje přední cíp mitrální chlopně, který zde tvoří překážku a obstrukci v toku krve. Toto může být příčinou synkop.
- diastolická dysfunkce – diastola je abnormální ve všech fázích. Izovolumická relaxace je prodloužená (komora se začne plnit později) s důsledku hypertrofie, morfologické i funkční dezorganizace kardiomyocytů a ischémie. Ischémie, hypertrofie myokardu i intersticiální fibróza zvyšují tuhost levé komory, důsledkem je zvýšení LVEDP a pokles koronárního průtoku. Toto může být příčinou dušnosti.
- arytmie – anatomickým substrátem je dezorganizace kardiomyocytů a fibróza (reentry) a spouštěčem LVOTO a ischémie. Časté jsou paroxysmální fibrilace síní, komorové extrasystoly a nesetrvalé komorové tachykardie (NSKT), největším rizikem jsou maligní arytmie a náhlá smrt (SD). Toto může být další příčinou synkop až náhlé smrti.
- ischémie = hypertrofie myokardu + abnormální a stenotické koronární arterioly + jejich zevní komprese hypertrofickým myokardem. Toto může být příčinou stenokardií.
- …až u jedné třetiny pacientů s HKMP dochází ke zvýšené klidové stimulaci mechanoreceptorů v levé komoře při abnormální tenzi ve stěně levé komory, díky tomu při zátěži ve vzpřímené poloze nedochází ke zvýšení krevního tlaku (TK), ale naopak k jeho snížení.
Klinický obraz – většina pacientů je asymptomatická a na HKMP se přijde náhodně. Pokud příznaky jsou, tak nejčastěji to je dušnost (90 % – diastolická dysfunkce), bolesti na hrudníku (75 % – ischémie) a synkopy (25 % – arytmie, LVOTO), méně palpitace (supraventrikulární arytmie, komorové extrasystoly). Klinický průběh choroby výrazně zhoršuje fibrilace síní (zhoršení všech příznaků). Při end-stage HKMP dochází k poklesu EF a dilataci levé komory, kdy se léčba významnější neliší od ostatních forem HFrEF.
CAVE První projevem HKMP může být SD, nejčastěji u vysoké zátěže (dosud nezjištěná vada u sportovců).
Fyzikální vyšetření – nález bývá často normální. Pokud jsou přítomny anomálie, pak je to zejména hlučný systolický šelest při levém okraji sterna, který se nešíří do axily ani do karotid. Tento šelest vzniká díky zúžení LVOT, tedy je závislý na preload (čím je náplň komor větší, tím je LVOT prostornější a šelest menší, čímž se liší od šelestu při aortální stenóze) – tedy všechny intervence, které vedou ke snížení plnění levé komory (Valsalvův manévr, podání nitrátů) vedou i ke zvýraznění šelestu, na rozdíl od šelestu při aortální stenóze.
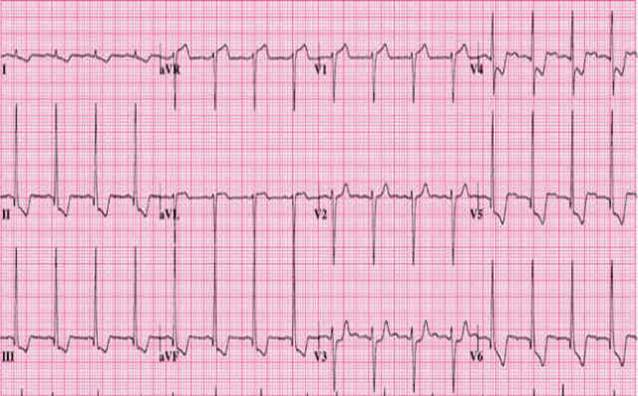
EKG – již při vstupním vyšetření je indikováno klidové EKG a 48 h EKG monitorace. Nález může být v podstatě jakýkoliv, ale většinou je EKG abnormální (sklon osy doleva, známky hypertrofie levé komory, LBBB, patologické Q a negativní T inferolaterálně (II, III, aVF, V3-6), známky P mitrale).
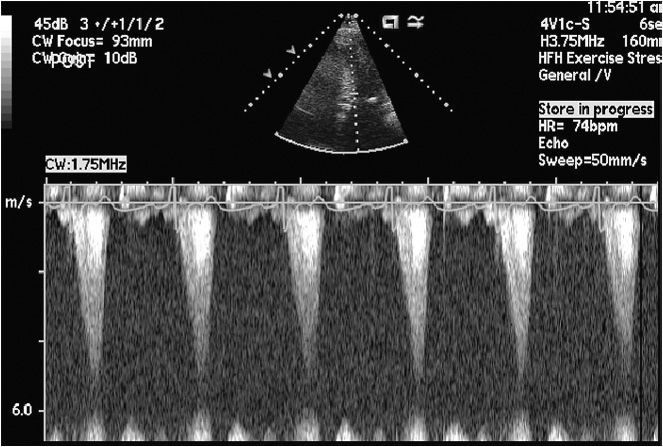
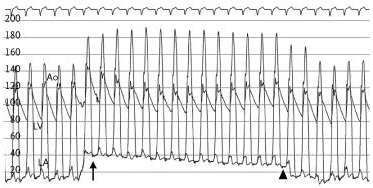
Echokardiografie – základní vyšetřovací metoda. Nejčastějším nálezem je asymetrické ztluštění jakéhokoliv segmentu myokardu, cut-off hodnota je 15 a více mm v terénu nedilatované (spíše malé) levé komory. Ke stanovení maximální tloušťky by měla být použita PSAX projekce na všech úrovních levé komory. Přítomnost LVOTO lze změřit pomocí CW, hranici pro HOKMP je gradient 30 mm Hg, hemodynamicky významný je > 50 mmHg. Tento gradient má na CW typicky „tvar dýky“. K indukci LVOTO lze použít Valsalvův manévr, nitráty, ale zátěžové echokardiografické vyšetření (při tomto nejen se zaměřením na maximální gradient ale i na zátěží indukovanou mitrální regurgitaci). Při špatné transthorakální vytěžitelnosti je indikováno MRI.
U většiny pacientů s HOKMP je přítomna mitrální regurgitace jako důsledek SAM (přední cíp je nasáván při systole do LVOT, logicky tedy nemůže pracovat dobře). Často dochází ke kontaktu v mitrálního cípu se septem .
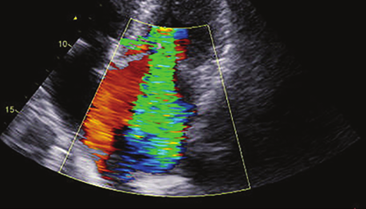
Echokardiograficky lze samozřejmě dále posoudit i ostatní hemodynamické parametry (diastolická dysfunkce apod.).
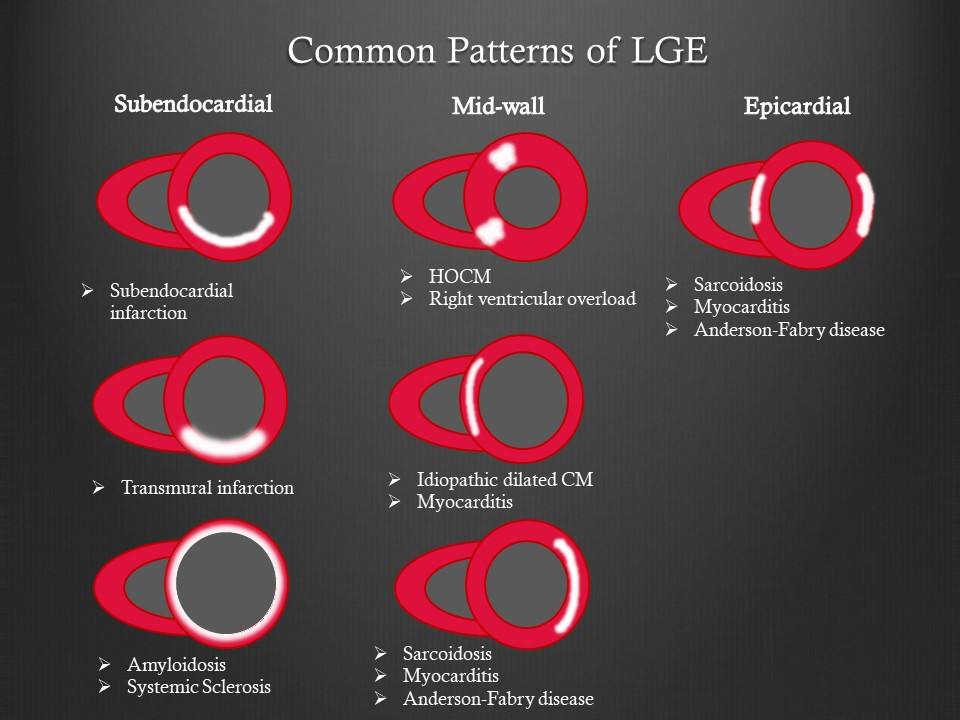
Magnetická rezonance – výhodou je, že dokáže určit hypertrofii i u hůře zobrazitelných a závažnějších forem HKMP (např. apikální), ale zejména je schopna určit stupeň fibrózy (pozdní sycení – LGE) hypertrofického myokardu což je důležité při posouzení rizika komorových arytmií a náhlé smrti.
Srdeční katetrizace – indikována k vyloučení ICHS a identifikaci vhodných septálních větví při alkoholové septální ablaci (ASA). Při té příležitosti je vhodné i invazivní stanovení nitrokomorového gradientů.
Ostatní – zátěžový test a nejlépe spiroergometrie mohou vysvětlit sníženou toleranci námahy (většina pacientů s HKMP i bez symptomů mají snížené VO2max) a častá je i abnromální tlaková reakce při zátěži ve vzpřímené poloze. Při podezření na metabolickou příčinu HKMP je indikována myokardiální biopsie.
Diagnostická kritéria HKMP (s výhodou lze použít u příbuzných pacienta s HKMP) – kdy diagnóza HKMP = 1 velké echo nebo 2 malá echo nebo 1 malé echo + 2 malé EKG.
- Echokardiografická
- velká
- ztluštění přední nebo části septa nebo zadní stěny na 13 mm a více nebo volné stěny na 15 mm a více.
- významný SAM.
- malá
- ztluštění přední nebo části septa nebo zadní stěny na 12 mm a více nebo volné stěny na 14 mm a více.
- nevýznamný SAM (není kontakt mitrální cíp – septum).
- velká
- EKG
- velká (…hypertrofie, patologické Q, negativní T)
- známky hypertrofie levé komory
- patologické Q v nejméně dvou svodech
- hluboké negativní T I, aVL, V3-6, II, III, aVF
- malá (…blok, malé repolarizační změny, S V2)
- kompletní raménkový blok nebo porucha vedení
- malé repolarizační změny
- hluboké (> 25 mm) ve V2
- velká (…hypertrofie, patologické Q, negativní T)
Riziková stratifikace – na základě studie publikované v roce 2014 bylo navrženo HCM Risk-SCD skóre, které na základě několika proměnných spočítá riziko náhlé smrti v následujících 5 letech (online zde: https://doc2do.com/hcm/webHCM.html). Dle toho lze stratifikovat pacienty na:
- nízké riziko – 5 leté riziko < 4 % – implantace ICD není indikována.
- střední riziko – 5 leté riziko 4 – 6 % – implantaci ICD lze zvážit.
- vysoké riziko – 5 leté riziko > 6 % – implantace ICD je indikována.
K rizikové stratifikaci není doporučena programovaná stimulace komor.
Terapie – obecně lze říci, že nejlépe lze ovlivnit symptomy vycházející z LVOTO (při gradientu > 50 mm Hg) než ostatních příčin (např. diastolická dysfunkce, ischémie apod.).
I. Režimová opatření
- vhodné je nevykonávat vysoce intenzivní sportovní aktivitu (zejména při rodinné anamnéze SD a nesetrvalých komorových arytmiích při EKG monitoraci), doporučuje se maximálně středně těžká fyzická zátěž a to až po zátěžovém EKG vyšetření (riziková je přítomnost arytmií a abnormální TK reakce na zátěž).
- při HOKMP je zásadní vyvarovat se dehydrataci a vazodilataci (není vhodná sauna a vyšší příjem alkoholu).
- zásadní je léčba rizikových faktorů aterosklerózy, protože současná ICHS výrazně zhoršuje prognózu pacientů.
II. Farmakoterapie – základem léčby HOKMP a symptomatické neobstruktivní HKMP je podávání negativně inotropních a pozitivně lusitropních léků. Indikovány jsou betablokátory (negativně ino- a chronotropní) do maximální tolerované dávky, při jejich kontraindikaci verapamil (pozitivně lusitropní a negativně inotropní). Verapamil je vhodný zejména při příznacích plynoucích z diastolické dysfunkce. Při arytmiích je preferován amiodaron. Při HOKMP se zachovalou EF je kontraindikován digoxin pro pozitivně inotropní efekt a zvýšení gradientu.
U většiny pacientů není indikována profylaktická farmakoterapie asymptomatických pacientů. U pacientů s HOKMP je zvýšení riziko IE, proto je indikována její standardní profylaxe.
III. Nefarmakologická terapie – pokud u pacientů s HOKMP > 50 mmHg nevede ani maximální farmakologická léčba ke kontrole příznaků jsou možné dvě následující možnosti:
- 1. Perkutánní alkoholová septální ablace (ASA) – indikována u septální formy HOKMP. Spočívá v katetrizační identifikaci vhodné septální větve, do které se aplikuje ethanol (identifikován pomocí periprocedurální echokardiografie). Dochází v podstatě k iatrogennímu septálnímu infarktu myokardu, který vede k projizvení a ztenčení původně hypertrofického bazálního septa a okamžitému poklesu tlakového gradientu v LVOT. Nejčastější komplikací je ve 30 – 50 % vznik úplného AV bloku, proto je vhodné mít pacienta zajištěného dočasnou kardiostimulací.
- 2. Chirurgická myektomie – provádí se nejčastěji transaortálně s odstraněním předem definovaného množství myokardu (5 – 10 g) z proximálního septa až k úponu předního papilárního svalu. Výkon je nevyhnutelně spojen s iLBBB nebo LBBB a není spojen s horší prognózou. Chirurgická myektomie je pravděpodobně vhodnější u pacientů < 65 let s výraznou hypertrofií a gradientem v LVOT.
- 3. Kardiostimulace – při selhání nebo odmítnutí všech předchozích postupů lze zvážit síňokomorovu sekvenční stimulaci se zkráceným AV intervalem (50 – 100 ms), což dle publikovaných dat snižuje gradient v LVOT.
- 4. ICD při HCM Risk-SCD > 6 %.
II. Nesarkomerická HKMP
Např. Fabryho choroba a amyloidóza (viz příslušné články).