Definice – záněty plicního parenchymu, které nejsou vyvolány infekcí (často používaný termín pneumonitida). Četnost je nižší než u infekčních pneumonií.
Etiologie – zařazují se sem různé stavy s poškozením plic vyvolaným vdechnutím cizorodých látek, plynů a par, imunitním poškozením nebo poškozením plic radioaktivním zářením.
Diagnostika – při vzniku respiračních potížích s přítomností plicního infiltrátu je anamnesticky důležitý údaj o okolnostech vzniku (aspirace?, inhalace toxických látek?, v tom případě je důležité toxikologické vyšetření a rozbor). Vhodné je ptát se na situace, při kterých dochází ke zhoršení stavu.
1. Aspirační pneumonie
Aspirace žaludečního obsahu
Vyvolávající příčinou jsou choroby jícnu (achalázie, striktura jícnu, ezofagotracheální / bronchiální píštěl), poruchy vědomí jakékoliv etiologie (choroby CNS, abusus alkoholu) nebo iatrogenně (tracheostomie, výplach žaludku). Na aseptický zánět často nasedá sekundární infekce (nejčastěji S. aureus, H. influenzae, G- střevní mikroflóra, anaeroby). Zánět je vyvolán kyselostí žaludečních šťáv, drážděním potravou a bakteriální kontaminací (Mendelsonův syndrom). Projevuje se náhle vzniklou dušností s cyanózou, krajně až ARDS. Na RTG je difuzní homogenní infiltrace až plicní edém. Nejčastější lokalizace pneumonie je v pravém dolním laloku. Léčba spočívá v okamžitém bronchoskopickém odsátí obsahu z plic, oxygenoterapii až intubaci s UPV, preventivně širokospektrá ATB. Po zaléčení lze očekávat zlepšení za 24 hodin. Na glukokortikoidy není jednotný názor. Důležitá je léčba základního onemocnění.
Aspirace vody
- sladká voda → hypoosmolalita → hypervolémie, hemodiluce s hemolýzou a následnou hypoxémií.
- slaná → hyperosmolalita → plicní edém.
Aspirace oleje
Vzniká po aspiraci minerálních rostlinných olejů (např. laxativa nebo nosní kapky – časté v době, kdy se do nosních kapek přidával parafín). Symptomatologie odpovídá množství aspirovaného oleje. Vyvolává lipoidní pneumonii s rizikem vzniku plicní fibrózy. V BAL jsou přítomny pěnovité makrofágy. Léčbou volby jsou glukokortikoidy, kyslík, event. ATB.
Speciálním typem je „pneumonie polykačů ohně“, která vzniká po aspiraci petroleje.
Aspirace benzínu, nafty, kerosinu
Pokud nemocný přežije aspiraci, dochází k akutnímu edému plic s následnou pneumonií, která má hnisavě nekrotizující charakter. V subakutním období vznikají opouzdřené dutiny (pneumatocele). Léčbou volby jsou glukokortikoidy, kyslík, event. ATB.

Aspirace cizího tělesa
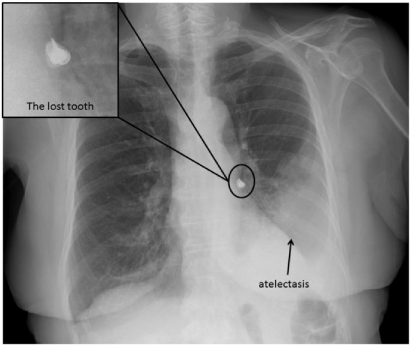
Aspirace malého tělesa může být klinicky němá s postupným vyvoláním recidivující pneumonie za stenózou, kdy infiltrace přetrvává i přes podání ATB. Velké těleso vyvolá sufokaci. Lokalizace je nejčastěji v pravém dolním laloku. RTG kontrastní těleso lze odhalit rentgenem. Diagnóza a léčba je bronchoskopie.
2. Inhalační pneumonie
Etiologie – vzniká po vdechnutí:
- toxických par a plynů (oxidy dusíku, Cl, ozón, toluen, NH4, fosgen, formaldehyd apod.).
- horkého vzduchu (hašení požárů).
Patofyziologie – oxidující plyny působí přímo na buněčné enzymy (NO2, Cl). Vzniklé látky narušují buněčné pH a vedou k destrukci buňky. Mizí pneumocyty I. typu, pneumocyty II. typu proliferují do vzniku intersticiální fibrózy. Důležitým faktorem je současná plicní komorbidita.
Klinický obraz – dobře rozpustné plyny maximálně poškozují nos, oči, horní dýchací cesty. Edém laryngu a bronchiální sliznice je příčinou dechových obtíží, stridoru a dráždivého kašle. Špatně rozpustné plyny alterují alveoly s rozvojem toxické exogenní alveolitidy. Alterace endotelových buněk vede k rozvoji plicního edému s latencí 8 – 12 hodin.
Terapie – zásadní je okamžité přerušení expozice, inhalace kyslíku (někdy nutná UPV), glukokortikoidy, profylaktické podávání ATB.
Inhalace zplodin hoření
Kombinace termického a chemického poškození. Nutná observace, protože se plicní poškození projevuje až s několikadenní latencí (asfyxie po inhalaci oxidu uhličitého, edém dýchacích cest za 8 – 36 hodin po inhalaci, ARDS). Léčebně se používá oxygenoterapie až UPV.
Nemoc silážníků
Při špatné ventilaci v silech se NO kumuluje ve vysoké koncentraci. Jeho inhalace vede ke vzniku akutní bronchiolitidy až plicního edému. V průběhu několika týdnů nález regreduje nebo se komplikuje bronchiolitidou. Choroba dobře reaguje na kortikoidy.
Inhalace ředidel nebo čisticích prostředků
Vznik plicního edémů u „čichačů“. Dobrá reakce na kortikoidy, někdy nutná oxygenoterapie až UPV.
Paraquatová plíce
Poškození plic koncentrovaným herbicidem paraquat při inhalaci a zejména ingesci (náhodné požití, sebevražedný úmysl), vstřebává se ale i přes kůži. V úvodu dochází k iritaci sliznic, po 3 – 5 dnech vzniká multiorgánové selhání a plicní edém, alveolitida, plicní fibróza a fatální respirační selhání (hlavní příčina smrti). Léčbou je snaha o rychlou eliminaci paraquatu (forsírováná diuréza, event. hemodialýza nebo hemoperfúze), pulzy glukokortikoidů, kyslík v nízké koncentraci. Mortalita je 70 %, při přežití je možná Tx plic.
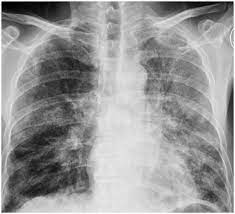
3. Postradiační pneumonitida
Etiologie – při radioterapii plicního karcinomu dochází k poškození i okolní plicní tkáně s projevem za 1 – 4 měsíce po terapii (u 7 % pacientů symptomaticky, u 43 % radiologicky).
Patofyziologie – gama záření působí tvorbu volných radikálů, které rozrušují buněčné membrány. Ovlivněny jsou rychle dělící se buňky, sestupně v pořadí bronchiální epitel → pneumocyty II. typu → endotelie → pneumocyty I. typu.
Klinický obraz – dušnost, suchý kašel, teplota s homogenním zastíněním a vzdušným bronchogramem odpovídajícím radiačnímu poli na RTG. Za 6 – 8 měsíců zde vzniká okrsek fibrózy, klinicky asymptomatický (při větším okrsku zasaženého parenchymu může vzniknout námahová dušnost). Průběh zhoršuje současná chemoterapie.
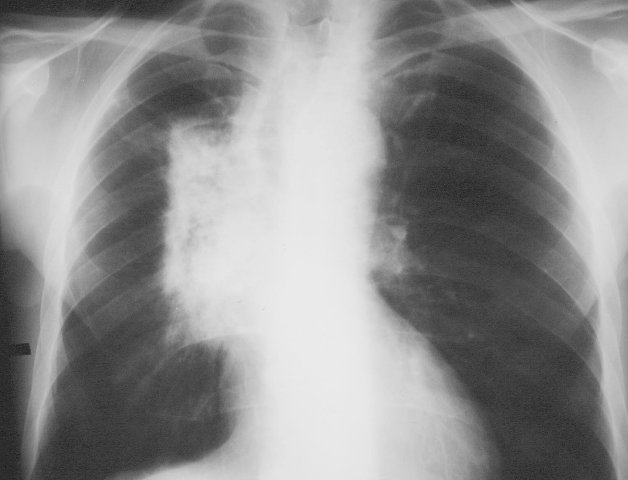
Terapie – glukokortikoidy, nejlépe v akutní fázi, ve fázi fibrózy již jen podpůrná léčba.
Prognóza – u vlastní pneumonitidy dobrá, přežití závisí na základním onemocnění.
4. Plicní eozinofilní syndromy
a) Hypersenzitivní pneumonitida
Úvod – hypersenzitivní pneumonitida (HP) je difúzní postižení plic, které je způsobeno opakovanou inhalací organických antigenů u predisponovaných jedinců. Onemocnění je pravděpodobně častější než idiopatická plicní fibróza (IPF), epidemiologická data ale chybí (odhaduje se, že 5 – 15 % osob vystavených vysoké koncentraci příslušných antigenů onemocní HP). Podobně je neucelená i klasifikace. Blíže viz. http://www.pneumologie.cz/guidelines/
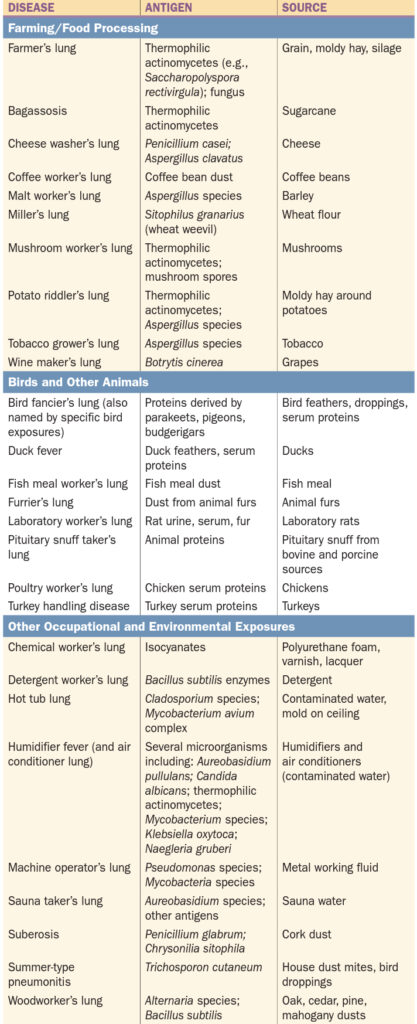
Etiologie – v podstatě jakýkoliv alergen může být spouštěčem HP. Četnými původci jsou aviární proteiny, houby, termofilní baktérie a nízkomolekulární chemikálie. Rozvoj HP byl popsán i v souvislosti s domácími vířivkami a bazény s horkou vodou („hot-tub lung“), saunami a zvlhčovači vzduchu.
Nejvíce ohrožení jsou farmáři, chovatelé ptáků, pracovníci v průmyslu a uživatelé vířivek, saun a wellness center.
Klinický obraz – průměrný interval mezi senzitizací a začátkem obtíží je individuální (i měsíce až roky). Choroba může mít následující formy:
- Akutní HP – obtíže se objeví za 4 – 8 hodin po intenzivní expozici antigenu. Nemocní udávají teplotu, třesavku, slabost, dušnost, tlak na hrudi a suchý kašel, často bolesti hlavy, artralgie a myalgie. Příznaky mizí za 1 – 2 dny a znovu se objevují po další expozici antigenu.
- Subakutní HP – nástup příznaků je více protrahovaný (řádově týdny).
- Chronická HP – vzniká spíše při dlouhodobé expozici antigenu. Příznaky se rozvíjí plíživě, pomalu progreduje námahová dušnost, slabost, nechutenství, hubnutí. Při neléčené HP se objevuje ireverzibilní plicní fibróza podvedoucí ke vzniku voštinovité plíce a cor pulmonale chronicum (v této fázi již podobné IPF).
Diagnostika – neexistuji bližší diagnostická kritéria.
Zásadní je souvislost vzniku akutní exacerbace HP se vznikem expozice určitému alergenu. U profesní expozice je typické vymizení příznaků přes víkend a po nástupu do práce v pondělí opětovné zhoršení.
- Extrémně důležitá je anamnéza směřující k identifikaci vyvolávajícího antigenu. V tomto směru může pomoci dotazník EAA (viz. guidelines ČPS, www viz výše).
- Fyzikální vyšetření s nálezem poslechového krepitu bilaterálně bazálně (méně než u IPF). Paličkovité prsty vznikají při chronické EAA.
- Radiologicky u akutní EAA spíše charakteru mléčného zastření, u subakutní EAA okrouhlé opacity, u chronické EAA retikulonodulace a voština.
- Funkční vyšetření plic obvykle prokazuje restrikční ventilační poruchu (někdy kombinovanou) a typicky v časných stádiích i zhoršení difúze (DLCO).
- Laboratorně lze detekovat specifické protilátky IgG proti vyvolávajícímu antigenu.
- V BAL obvykle dominují CD8+ lymfocyty (nízký imunoregulační index CD4+:CD8+ < 1).
- Plicní biopsie je indikována při diagnostických rozpacích. Typický je nález granulomů v dýchacích cestách, které jsou (na rozdíl od sarkoidózy) méně ohraničené.
Terapie – nejdůležitější je identifikace vyvolávajícího antigenu a zamezení jeho další expozici. V akutní fázi, při těžkém průběhu nebo progresi onemocnění jsou indikovány glukokortikoidy ve střední dávce (0,5 – 1 mg prednisonu/kg) na 2 týdny s postupnýmm snížením dávky během dalších 4 týdnů.
Prognóza – akutní EAA má dobrou prognózu, při chronické EAA s fibrózou je prognóza horší.
b) Plicní infiltráty s eozinofilií
Základem je rozhodnutí, zda jsou eozinofilní plicní infiltráty primární nebo jsou způsobeny sekundárně jako reakce na léky (nitrofurantoin, NSAID…), infekci, malignitu nebo jiné plicní choroby (např. asthma). Typická je infiltrace plic eozinofily, zásadním cytokinem je pravděpodobně IL-5.
Akutní eozinofilní pneumonie
Projevuje se kašlem, dušností, schváceností, myalgiemi, nočními poty, bazálně slyšitelnými chrůpky a horečkou. Počátek je poměrně náhlý a doschází k respirační insuficienci, často vyžadující mechanickou ventilaci. Nejčastěji postihuje muže mladšího věku, často nedávným zahájením kouření nebo nové expozici alergenu (např. po domácí rekonstrukci s pobytem v prachu). Choroba je často zaměňována za ARDS, až do chvíle, než se provede BAL, kde se prokáže > 25 % eozinofilů.
CAVE Eozinofilie není přítomna od počátku, vzniká až po 7 – 30 dnech od nástupu nemoci (eozinofily v periferní krvi jsou obvykle cca 1700/ul).
Dle diagnostických kritérií jde o akutní febrilní stav s respiračními příznaky a hypoxémií trvající < 1 měsíc a projevující se difuzními infiltráty na RTG. V BAL je eozinofilie > 25 %, ale zároveň je vyloučena parazitická, mykotická i jiná infekce i vliv léku, který působí eozinofilii. Je dobrá a rychlá reakce na kortikosteroidy a po jejich vysazení dochází k rychlému relapsu.
Mimo eozinofilie je přítomno i nespecifické zvýšení FW, CRP i IgE. Na rozdíl od ARDS není přítomno selhání jiných orgánů než plic. Choroba má výbornou prognózu. Základem je symptomatická léčba a glukokortikoidy.
Chronická eozinofilní pneumonie
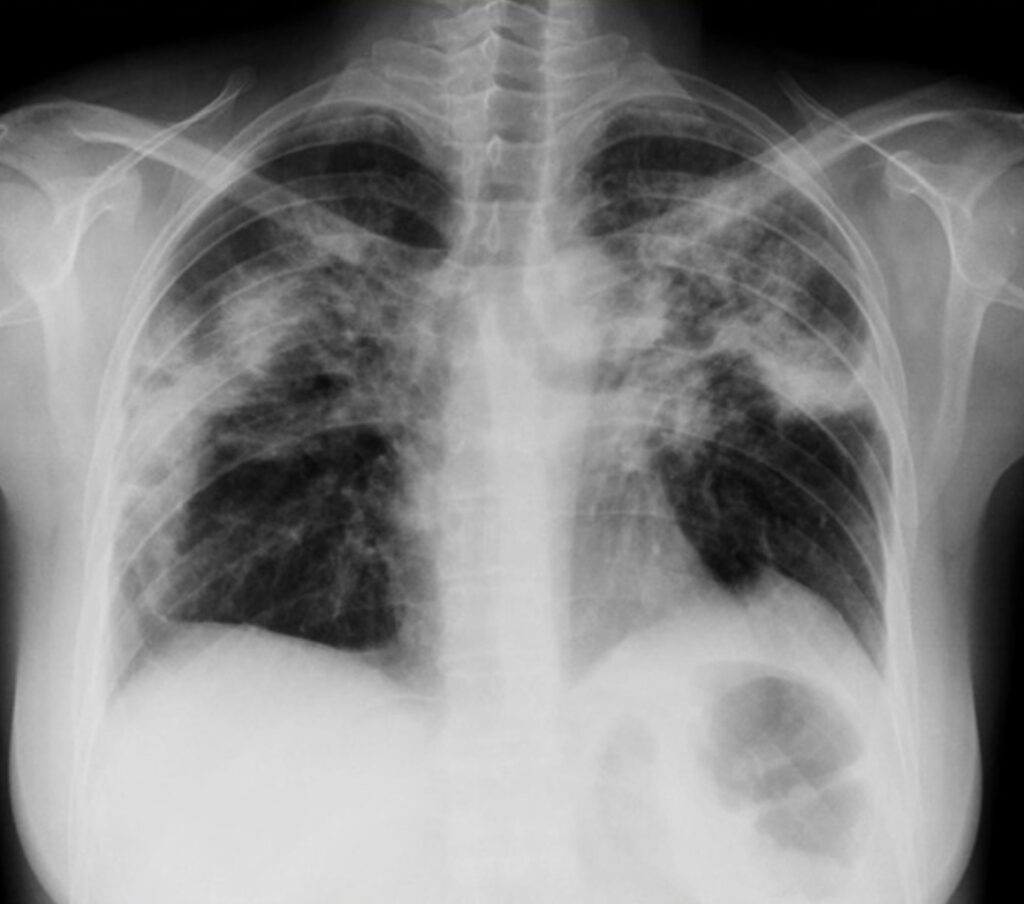
Chronická nemoc postihující nejčastěji ženy nekuřačky ve věku okolo 45 let, většinou s anamnézou alergie a asthmatu (podobně jako EGPA). Anamnéza trvá týdny až měsíce s necharakteristickými příznaky (kašel, slabé horečky, progredující dušnost, váhový úbytke, pískoty, únava a noční poty). Na RTG je nález „fotograficky negativního plicního edému“ (zastínění je na periferii a zejména v horních polích), který je poměrně specifický, ale je přítomen u < 25 % pacientů).
c) Eosinofilní granulomatóza s polyangitidou
Definice – dříve syndrom Churg – Straussové. Onemocnění charakterizované asthmatem + hypereozinofilií v periferní krvi + tkáňovou eozinofilií + histopatologickým obrazem nekrotizující vaskulitidy a extravaskulárních granulomů. Na rozdíl od polyarteritis nodosa postihuje spíše cévy malého kalibru a souvisí s asthma bronchiale.
Epidemiologie – incidence je velmi nízká (1:200 tisíc – 2 milióny/rok), prevalence 1: 100 tisíc, nejčastěji ve středním věku a lehce častěji muže.
Patogeneze – nejasná, převaha Th2 imunologické odpovědi (určitou roli hraje i Th1 se vznikem granulomů). Přítomno snížení T regulačních lymfocytů produkujících IL-10. Časté protilátky cANCA, které zjištěny u cca poloviny nemocných.
Klinický obraz – několik fází:
- Prodromální – chronická rhinitis s nosními polypy či astmatem, může trvat řadu let.
- Časná systémová fáze – objevují se eozinofilie a prchavé plicní infiltráty.
- Pozdní systémová fáze:
- nespecifické – horečka s váhovým úbytkem
- plicní – masivní infiltráty bez rozpadu, někdy difuzní postižení intersticia
- ledvin – erytrocyturie ev. i malá proteinurie, u malé části pacientů selhání ledvin
- srdeční – myokarditida s rozvojem srdečního selhání
- nervové – periferní mononeuropatie
Mimotechnická pomůcka pro zapamotování mononeuropatie: WARDS PLC (Wegener, Amyloidóza/AIDS, Revmatoidní artritida, Diabetes, Sarkoidóza, Polyarteritis nodosa, Lepra, Carcinom/Churg Strauss).
Diagnostika – kritéria (v současnosti se od těchto kritérií postupně ustupuje a diagnostika se soustředí na klinický obraz). Diagnóza je dána splněním minimálně 4 ze 6 kritérií:
- Astma bronchiale
- Prchavé plicní infiltráty dle RTG S+P
- Postižení vedlejších nosních dutin
- Eozinofilie
- Extravaskulární eosinofilní infiltráty (biopticky verifikované)
- Periferní neuropatie
- Laboratorní vyšetření: ↑ FW, CRP, leukocyty, ↓ hemoglobin (normocytární normochromní anémie), cANCA pozitivita – proti proteináze 3
- Biopsie – zánětlivé změny na středních a malých cévách s eozinofilním infiltrátem
Terapie
- 1. volba – glukokortikoidy (prednison 40 – 60 mg/kg/den s postupnou detrakcí)
- 2. volba – u pacientů s těžším průběhem nebo kortikorezistentních cyklofosfamid
Prognóza – před zavedením kortikoidů umírala polovina pacientů do 3 měsíců od prvních projevů vaskulitidy a 5 let přežívalo méně než 5 % pacientů. V současnosti pět let přežívá díky kombinované léčbě více než 75 % nemocných. Nejčastější příčinou smrti v akutní fázi onemocnění je infarkt myokardu nebo srdeční selhání. Výskyt pozdních relapsů nemoci je možný, ale není tak častý jako u jiných vaskulitid.
d) Ostatní příčiny eozinofilie
Hypereozinofilní syndrom – definován jako trvalá eozinofilie > 1500/ul při vyloučení sekundární příčiny (léky, nádor, alergie, infekce a systémové choroby). Příčinou je např. mutace PDGFR-alfa, -beta, JAK2 a FGFR. vyskytuje se častěji u mužů ve věku 20 – 50 let s možnosti infiltrací řady orgánů, např. srdce, GIT, jater, ledvin, kloubů a kůže. V případě postižení plic jsou vysoké hladiny eozinofilů v krvi, BAL i plicním parenchymu. Léčbou volby jsou kortikoidy, které mají ale efektu u < 50 % pacientů.
Alergická bronchopulmonální aspergilóza – eozinofilní plicní syndrom jako následek alergické senzitizace na antigeny aspergilů, častá u cystické fibrózy. Projevuje se jako asthma, s event. expektorací hnědavého hlenu. projevuje se periferní eozinofilií a zvýšením cirkulujících IgE, pozitivitě kožního testu na antigen aspergila a přítomnosti specifických cirkulujících protilátek IgG a IgE proti aspergilům. Základem léčby je inhalační terapie podobně jako u asthmatu, při reszistemci systémové kortikoidy. Antimykotika (flukonazol, vorikonazol) lze podat k redukci antigenní nálože jako 4 týdenní kůru.
Löfflerův syndrom – přechodné samovolně ustupující onemocnění (mizí řádově v týdnech) s plicními infiltráty a eozinofilií u asymptomatických nebo minimálně symptomatických pacientů. Příčinou jsou paraziti migrující přes plicní parenchym (ascaris, toxocara, strongyloides).
Léky – nejčastěji NSAID a antibiotika, nejvíce nitrofurantoin.Léčbou je odstranění léku z medikace, při závažných příznacích glukokortikoidy. Eozinofilní infiltráty vznikají někdy i po radioterapii pro karcinom prsu.