Divertikulóza
Epidemiologie
- prevalence – divertikulóza v USA postihuje 70 % pacientů starších 80 let. Pouze 20 % z nich je symptomatických, 1 – 2 % vyžaduje hospitalizaci a ˂ 1 % chirurgický zákrok. Dříve byla divertikulóza doménou rozvinutých zemí, nyní, v období, kdy se nezdravý, „západní“ styl stravování dostává do rozvojových zemí, prevalence stoupá i zde. Důkazem je, že imigranti do USA onemocní divertikulózou stejně často jako nativní Američané. Zvláštností je, že u Asiatů bývá v 70 % postiženo cékum a colon ascendens.
- pohlaví – obě pohlaví jsou postižena stejně často, u mužů vzniká v dřívějším věku.
- věk – střední věk manifestace je 59 let s přesunem do mladších věkových skupin.
Anatomie a patofyziologie – ve střevě jsou přítomny dva různé typy divertiklů. Stěna pravých divertiklů je složena z celé střevní stěny, zatímco falešné divertikly (pseudodivertikly) vznikají protruzí pouhé sliznice a submukózy přes muscularis propria tlustého střeva. Nejčastěji bývají postiženy sigmoideum a colon descendens, přičemž rektum nebývá nikdy postiženo. Ke vzniku divertiklu dochází následující cestou:
- 1. Zácpa a stolice s vysokým obsahem tuku vede k obtížnému postupu stolice a aby k němu došlo, jsou v poměrně svalnatém sigmatu nutné jeho velmi silné kontrakce.
- 2. Díky zvýšenému intralumunálnímu tlaku jsou vasa recti komprimovány se vznikem ischemie a následného krvácení nebo eroze. Určitou roli hraje i chronický zánět a degenerace slizničních neuronů střeva.
- 3. Ke vzniku divertiklu dochází v bodu, kdy nutriční tepny nebo vasa recta penetrují přes muscularis propria, čímž naruší integritu stěny tlustého střeva s jejím oslabením, přes které prolabuje střevní stěna.
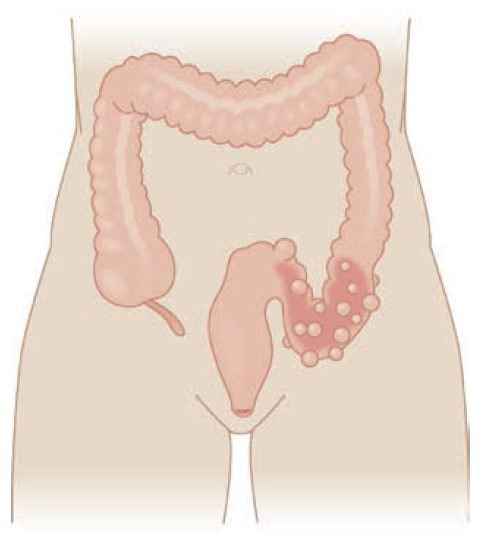
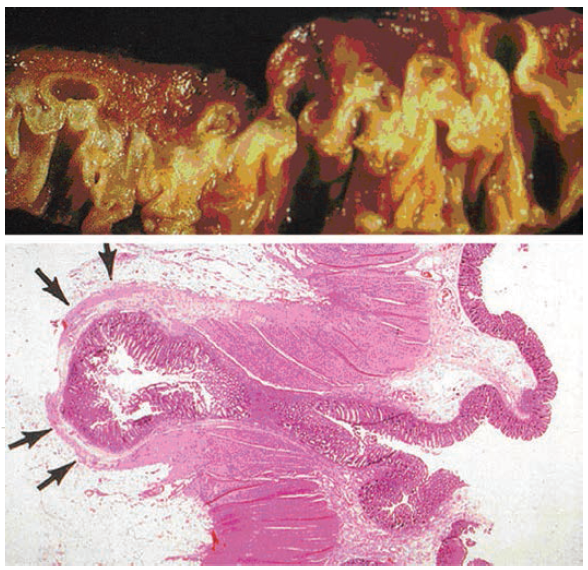
Krvácení z divertiklů – nejčastější příčinou rektorágie u pacientů ˃ 60 let jsou právě divertikly tlustého střeva, ale pouze u 20 % jedinců s divertikulózou ke krvácení dochází. Toto po zajištění „klidu střeva“ (nic per os, žádná střevní prokinetika) většinou samo ustává, ale u 25 % jedinců dochází někdy v životě k jeho recidivě. Riziko krvácení zvyšuje hypertenze, ateroskleróza, diabetes mellitus, obezita a užívání NSAID, antiagregační a antikoagulační léčby. Ke zjištění místa primárního krvácení může pomoci kolonoskopie, CT angiografie, scintigrafie se značenými erytrocyty nebo angiografie mezenteriálních tepen. Je několik možností terapie:
- 1. Pokud je pacient stabilní, je nejspolehlivějším vyšetřením angiografie mezenteriálních tepen, při které může být proveden terapeutický coiling postižené tepny s úspěšností 80 % pacient by měl být poté brzo zkontrolován kolonoskopicky k časné diagnostice event., iatrogenně způsobené ischemické kolitidy. Rizika procedury jsou poměrně nízká (ischemie tlustého střeva ˂ 10 %, recidiva krvácení ˂ 25 %, dlouhodobý úspěch colilingu ˃ 50 %).
- 2. Alternativou je provedení chirurgické resekce postiženého segmentu tlustého střeva, což bývá výhodné zejména u pacientů s nutností chronické antikoagulační terapie. Tato metoda je indikována i při nestabilitě pacienta, nebo nutnosti podání více než 6 jednotek krve během posledních 24 hodin. Pokud nelze identifikovat zdroj krvácení může být jediným řešením provedení subtotální kolektomie. Pokud nejsou přítomny výrazné komorbidity je vhodné výkon ukončit primární reanastomózou (častější leak v anastomóze je statisticky popisován při nutnosti podání více než 10 jednotek krve).
Divertikulitida
Divertikulitida může mít různý průběh. Akutní nekomplikovaná divertikulitida se projevuje nechutenstvím, horečkou, bolestí levého dolního břišního kvadrantu a zácpou. V < 25 % pacient přichází až ve stádiu difuzní peritonitidy, která značí pravděpodobnou rupturu divertiklu. V laboratorním obraze je leukocytóza s posunem doleva, při obrovském divertiklu lze nalézt hladinku na prostém snímku břicha. K diagnostice je nejlepší CT břicha s kontrastem, který prokáže ztluštění stěny tlustého střeva > 4 mm a zánětlivé prosáknutí perikolického tuku, při abscesu lze nalézt kolekci tekutiny. Divertikulitida může napodobovat syndrom dráždivého tračníku, ovariální cysty, endometrióza, apendicitida nebo jiný zdroj pánevního zánětu. Platí, že pacienti bez horečky nebo leukocytózy a s normálním CT nálezem nemají divertikulitidu.
CAVE Divertikulitida a kolorektální karcinom mohou probíhat paralelně. Zásadou je proto provedení kolonoskopie cca 6 týdnů po zklidnění akutního zánětu.
Současná přítomnost abscesu, perforace nebo vzácněji píštěle se označuje jako komplikovaná divertikulitida. vyskytuje se častěji u kuřáků.
- perforace – klasifikuje se podle Hincheyho. Toto schéma bylo vyvinuto k předpovědi dalšího průběhu po chirurgické terapii komplikované divertikulitidy:
- stupeň I – perforovaná divertikulitida s lokalizovaným parakolickým abscesem.
- stupeň II – perforovaná divertikulitida se spontánním uzávěrem a vznikem vzdáleného abscesu.
- stupeň III – nekomunikující perforovaná divertikulitida se sterkorální peritonitidou (krček divertiklu je uzavřen a kontrastní látka proto neuniká).
- stupeň IV – komunikující perforace krčku se sterkorální peritonitidou (krček divertiklu je otevřen a kontrastní látka uniká mimo divertikl).
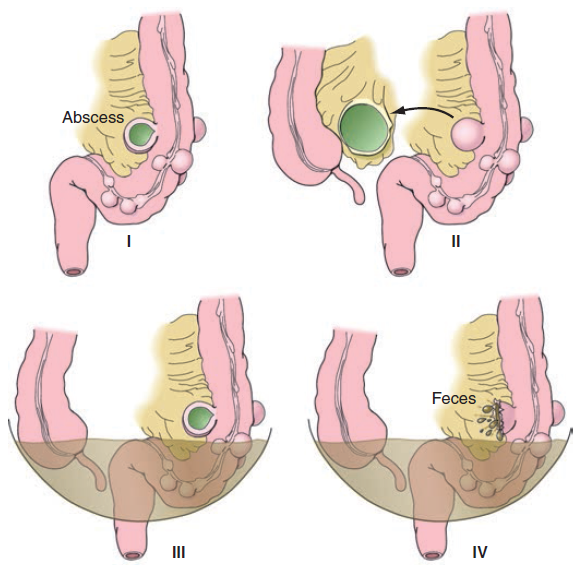
- perikolický absces – projevuje se napnutím břicha se známkami lokalizované peritonitidy.
- píštěl – vzácnější, může být kožní, vaginální (častěji u žen po hysterektomii) nebo močová (nález pneumaturie).
Terapie
1. Asymptomatická divertikulóza – základem terapie nekomplikované divertikulózy je:
- dieta s vysokým obsahem vlákniny (nejméně 30 g denně), často i s podáváním vlákniny jako doplňků výživy. Historická doporučení, aby pacienti přestaly jíst ořechy lze nyní považovat za anekdotu…
- vhodné je přestat kouřit.
2. Nekomplikovaná divertikulitida
- 2a Terapie akutní divertikulitidy – nekomplikovaná divertikulitida s projevy zánětu a infekce by měla být úvodem léčena pomocí střevního klidu. Nyní jsou k dispozici data potvrzující bezpečnost nepodávání antibiotik úvodem (studie AVOD, DIABOLO). U jinak zdravých jedinců lze postupovat ambulantně, při nemožnosti užívat orální terapii, závažných komorbiditach nebo při komplikující divertikulitidě je lepší postupovat za hospitalizace. Zásady terapie:
- dodržování „střevního klidu“
- u závažnějšího průběhu antibiotická terapie cefalosporiny 3. generace nebo ciprofloxacin + metronidazol (pokrytí G- bakterií a anaerobů, bohužel již ne enterokoků, proto při nedostatečném efektu terapie je nutné přidat ampicilin). Alternativně lze podat v monoterapii piperacilin/tazobaktam.
- vhodné je přestat kouřit.
- 2b Udržovací terapie – divertikulární nemoc je nyní považována za chronický zánět nízké intenzity, po zvládnutí akutní fáze by proto měla být zavedena chronická terapie:
- u nekomplikované divertikulózy může být účinný mesalazin, při průkazu zvýšeného zánětu (pozitivní CRP) je ale již neefektivní.
- určitý efekt mohou mít i probiotika s obsahem Lactobacillus acidophillus a Bifidobacterium, ale recentní meta analýza neprokázala větší benefit.
- u nekomplikované symptomatické divertikulitidy vede podávání rifaximinu (širokospektré nevstřebatelné antibiotikum) ke snížení četnosti symptomů o cca 30 %.
3. Chirurgická terapie – pooperační mortalita závisí na předoperační klasifikaci ASA (American Society of Anesthesiologist) a přítomnosti orgánového selhávání. U pacientů s nízkým rizikem (ASA I a II) může být chirurgická terapie nabídnuta při neefektivnosti režimových a farmakologických opatření, u závažnějších komorbidit je nutné si uvědomit, že pacienti na imunosupresivní terapii, s chronickou renálním selháním a u systémových vaskulitid mají 5x vyšší riziko perforace. Studie DIRECT prokázala, že chirurgická resekce byla při 5 letém follow-up spojena s lepší kvalitou života. Cílem chirurgické terapie je kontrola sepse, eliminace komplikací (např. fistula, obstrukce), odstranění postiženého segmentu střeva a obnovení jeho kontinuity. Je indikována u všech komplikovaných divertikulitid.
3a Chirurgická terapie nekomplikovaných divertikulitid – volbou je laparoskopická/otevřená resekce postižené části střeva a end-to-end anastomóza.
3b Chirurgická terapie komplikovaných divertikulitid – lze zvolit několik výkonů:
1. Laparoskopická revize s výplachem a drenáží (vyšší riziko reoperace než u otevřených výkonů).
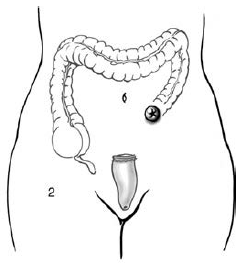
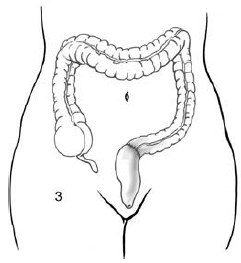
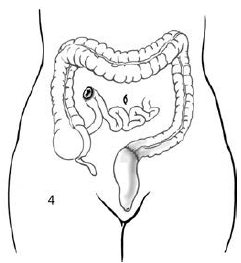
Volba výkonu:
Hinchey I a II – lze zvládnout perkutánní drenáží s následnou resekcí a anastomózou po cca 6 týdnech. Dle guidelines American Society of Colon and Rectal Surgeons je u divertikulárních abscesů:
- ˃ 3 cm – antibiotická terapie + CT navigovaná perkutnánní drenáž
- ˂ 3 cm – pouze antibiotická terapie bez drenáže
Kontraindikací perkutánní drenáže je špatný anatomický přístup, pneumoperitoneum, sterkorální peritonitida.Dle jedné nerandomizované studie vedl konzervativní postup izolovaného parakolického abscesu (Hinchey I) k recidivě během 2 let ve 20 %. Při vzdálených abscesech (Hinchey II) bylo ve více než 80 % potřeba chirurgická resekce pro recidivu zánětu. Při selhání anastomózy bývá indikován urgentní chirurgický výkon, nejčastěji Hartmannova operace.
Hinchey III – správný postup je stále předmětem debaty. Dříve byl výkonem volby Hartmannova operace, nedávné studie testovaly možnost limitovaného výkonu (peritoneální laváž a drenáž), nicméně byla prokázáno vyšší riziko reoparece pro pokračující peritonitidu.
Hinchey IV – neměla být snaha o žádnou anastomózu, i zde ale platí, že limitovaný výkon je spojen s nižší mortalitou.
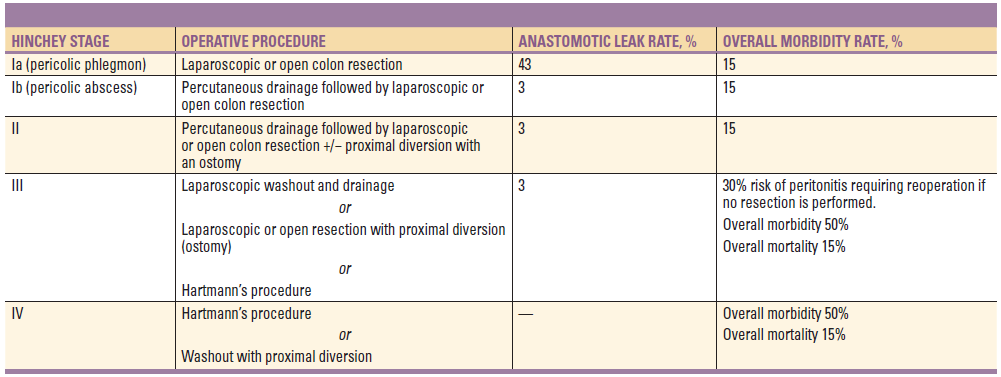
Po chirurgické resekci jsou u cca 10 % pacientů přítomny příznaky abdominálního dyskomfortu, nejčastěji při nedostatečné chirurgické resekci (současně je i dvojnásobné riziko recidivy).
Prolaps rekta
Epidemiologie – 6x častější u žen než u mužů, incidence vrcholí ve věku ˃ 60 let.
Ženy s prolapsem rekta mají častější výskyt ostatních poruch pánevního dna (např. močovou inkontinenci, rektokéle, cystokéle a enterokéle), dále je častěji současný Ehlers-Danlosův syndrom, solitární vřed rekta, vrozený hypotyreoidismus, Hirschprungova chorobu, demence, mentální retardace a schizofrenie.
CAVE 20 % dětí s prolapsem rekta má cystickou fibrózu, proto by všechny děti s prolapsem měly podstoupit potní test.
Anatomie a patofyziologie – prolaps rekta je cirkumferenciální protruze střevní stěny v celé její šířce přes anální ústí. Bývá spojen s redundancí sigmatu, uvolněním tonu pánve nebo hlubokým cavum Douglasi. Patofyziologické hypotézy:
- původně se uvažovalo, že časnou známkou prolapsu je intususcepce proximální a střední části rekta. Sledování pacientů ovšem tuto domněnku ukázalo jako velmi nepravděpodobnou, protože jen u 1 pacienta z 38 tento vnitřním prolaps během 5 let progreduje do plně vyjádřeného prolapsu rekta.
- dále se zvažuje, že prolaps rekta vzniká následkem poškození nervů zásobujících pánevní dno nebo pudendálních nervů s oslabením svalů pánevního dna, včetně zevního análního svěrače. Oboustranné poškození pudendálních nervů je spjato s prolapsem rekta významně častěji než jednostranné.
Klinický obraz – při vnějším prolapsu si většina pacientů stěžuje na masu v oblasti anu, čerstvou krev ve stolici a zhoršení perianální hygieny. Vzniká obvykle při defekaci a reponuje se spontánně nebo manuálně pacientem. Zácpa je přítomna u 30 – 67 % a inkontinence stolice u 50 – 70 % pacientů. Při vnitřním prolapsu mohou být přítomny jak zácpa i inkontinence, obstrukce anu (30 %), porucha motility tlustého střeva při snaze o defekaci proti uzavřenému pánevnímu dnu (10 %) a solitární rektální vřed (12 %).
Ke zhodnocení prolapsu je vhodné podání klysmatu, které umožní jeho protruzi. Vždy je potřeba rozlišovat prolaps celé stěny rekta a izolovaný slizniční prolaps při hemoroidech (pro ten jsou typické radiální perianální rýhy při zvýšené volnosti pojivové tkáně mezi sliznicí a svalovou vrstvou).
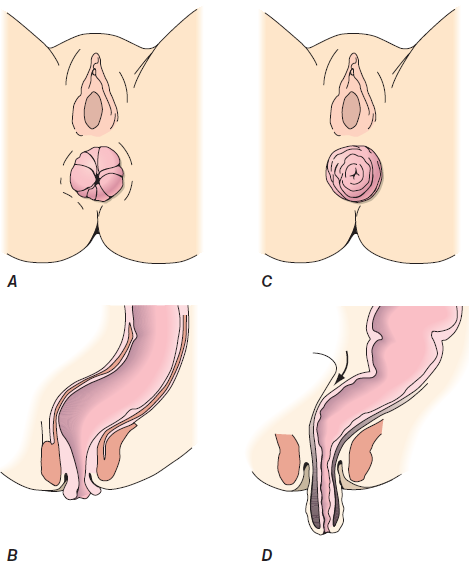
C, D. Prolaps celé stěny rekta s redundancí rektosigmatu a cavum Douglasi.
Diagnostika
1. K došetření příčin prolapsu jsou vhodné cystoproktografie (k vyloučení poruchy pánevního dna) a kolonoskopie k vyloučení polypu nebo malignity).
2. Při chronické zácpě by měl být doplněn i defekační proktogram a stanoven tranzitní čas tlustým střevem (sitz marker study) k vyloučení poruchy motility tlustého střeva (při pozitivním nálezu je na prostém RTG břicha retence ˃ 20 % markerů po 5 dnech od jeho požití.
3. Při inkontinenci stolice je vhodné doplnění endoanálního ultrazvuku a manometrického vyšetření, včetně testu pudendální inervace análních svěračů
Terapie
1. Farmakoterapie a režimová opatření – možnosti konzervativního postupu při prolapsu rekta jsou omezené a patří k nim změkčení stolice a suplementace vlákniny k co nejšetrnější defekaci.
2. Chirurgická terapie – základ léčby prolapsu rekta. Existují dva přístupy:
a) Transabdominální přístup je spojen s menším rizikem recidivy, ale rizikovější u pacientů s více komorbiditami. Cílem je znovunastolení normálních anatomických poměrů v břiše, odstranění nadbytečného střeva a uchycení rekta k presakrální fascii. Některé výkony lze provádět laparoskopicky nebo nověji pomocí robotické chirurgie:
- presakrální sutura
- rektopexe pomocí síťky (Ribsteinova operace) s/bez resekcí nadbytečného sigmatu (Frykman-Goldberg). Tato resekce bývá indikována při obstrukci nebo chronické zácpě. Při úplné poruše motility a pozitivitě sitz marker study může být doplněna o subtotální kolektomii s anastomózou ilea k sigmoideu nebo rektu jako ultimum refugium.
- ventrální rektopexe je efektivní metodou při kompletním prolapsu, při kterém není nutná resekce sigmatu. Výkon má nejlepší funkční efekt.
- proktektomie s endsigmoidální kolostomií je konečným výkonem u jinak neřešitelných prolapsů
b) Transperineální přístup je šetrnější k pacientovi. Nejčastější je:
- transanální proktektomie (Altmeierova operace)
- slizniční proktektomie (Delormeho operace)
- obkroužení anu Tirschovým drátem
3) Léčba vnitřního prolapsu – při prokázání vnitřního prolapsu může být vyzkoušen biofeedback, který ale bývá úspěšný pouze u 30 % pacientů, u zbytku je nutné přistoupit k chirurgické korekci:
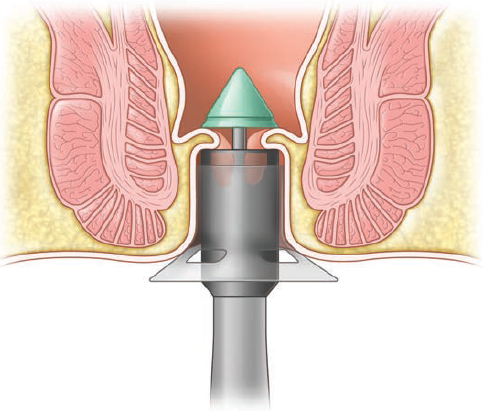
- STARR (Stapled TransAnal Rectal Resection) je prováděn transanálním přístupem. Do anu se vloží cirkulární stapler, který liguje vnitřní prolaps.
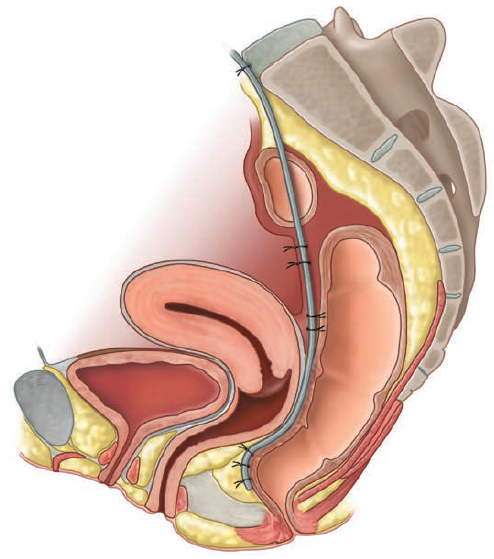
- LVE (Laparoscopic Ventral Rectopexy) se provádí transabdominálně. Na levé straně rektosigmoideální junkce se pronikne do břišní dutiny a odtud se dále laparoskopicky pokračuje do cavum Douglasi. Mobilizace rekta se neprovádí, proto ani nedochází k poranění autonomních nervů. Poté je na přední a laterální část rekta, vaginální fornix a sakrální promontorium fixována síťka, která umožní uzávěr rektovaginálního septa a korekci vnitřního prolapsu.U obou procedur je velmi nízké riziko recidivy (˂ 10 %/rok) s velmi častým zlepšením příznaků (˃ 75 %).
Inkontinence stolice
Definice – mimovolný odchod stolice, který se objevuje po dobu delší než 1 měsíc a ve věku vyšším než 4 roky.
Epidemiologie – v USA je prevalence 0,5 – 11 %, většinou u žen (více u rodiček), nejčastěji ve věku ˃ 65 let. Polovina pacientů mají zároveň inkontinenci moče i stolice.
Etiologie
1. Poškození pánevního dna během těhotenství nebo porodu – příčinou většiny případů je poškození pánevního dna při těhotenství nebo porodu. Rizikovým faktorem je prodloužení porodu, použití porodních kleští a potřeba epiziotomie. U 32 % pacientů je zjištěna i nezávislá porucha svěrače.
CAVE Ke vzniku inkontinence může dojít i po více než dvaceti letech od poranění!
2. Ostatní – k ostatním příčinám patří neurologické poruchy, sklerodermie, myopatie, myasthenia gravis, hypotyreóza, diabetes syndrom dráždivého tračníku a těžký průjem.
Anatomie – anální svěrač je složen z vnitřního sfinkteru složeného z hladké cirkulární svaloviny, která je pokračováním stěny rekta. Je inervován vlákny plexus myentericus a není proto ovládaný vůlí a vnějšího sfinkteru, který vzniká pokračováním vláken musculus levator ani. Je inervován pudendálními nervy a je proto ovládán vůlí.
Patofyziologie – k poranění dochází natažením pudendálních nervů, kdykoliv během těhotenství nebo natržením ventrální části svalových vláken během porodu (lze prokázat na endoanálním ultrazvuku).
Klinický obraz – fekální inkontinence může mít různý stupeň závažnosti a vždy vede ke zhoršení perianální hygieny. Mírné formy jsou omezeny na plynatost s občasným odchodem tekuté stolice, při závažných formách jsou časté odchody tuhé stolice. Závažné formy mají dopad na psychiku pacienta (časté deprese) a zhoršují kvalitu života.
Diagnostika
1. Anamnéza a fyzikální vyšetření – i zde je základem důkladná anamnéza i fyzikální vyšetření, včetně vyšetření per rectum. Slabý tonus svěrače i „mrkací reflex anu“ (S1) vede k podezření na neurologickou příčinu, anální jizvy mohou indikovat poškození svěrače při předchozím chirurgickém výkonu.
2 Přístrojová diagnostika
Anorektální manometrie (ARM) – při ARM se měří klidový a maximální tlaky uvnitř análního kanálu (injekcí vody do střeva pomocí intraluminálního katetru). Současná technologie používá systém s 12 katetry umožňující high-resolution 3D zobrazení tlakových poměrů v rektu.
Terminální motorickou latenci pudendálních nervů (PNTML) – pomocí elektrody umístěné na prstu vyšetřujícího a zavedené do análního kanálu se stimuluje svěrač a měří se motorická odpověď. Při poškození pudendálních nervů je tato odpověď prodloužená.
Endoanální ultrazvuk hodnotí poškození svěrače před event. chirurgickou rekonstrukcí.
Variantou je i MRI, která se ale při diagnostice fekální inkontinence rutinně nepoužívá. Fekální inkontinence je velmi často provázena i močovou inkontinencí nebo prolapsem jiných orgánů přes dno pánevní. Součástí vyšetřovacího algoritmu by proto mělo být minimálně i důkladné urologické a gynekologické vyšetření, popřípadě dynamická MRI pánve.
Terapie
1. Základem je snaha o zvětšení a zahuštění stolice se zlepšením sensingu v oblasti anu. Lze použít vlákninu, loperamid, difenoxylát a vazače žlučových kyselin. Tato opatření zahušťují stolici a prodlužují frekvenci stolic. Mohou být prospěšná při nezávažné formě inkontinence.
2. Další bezpečnou možností je biofeedback s variabilním úspěchem (velmi záleží na motivaci pacienta), kdy většina pacientů popisuje alespoň částečné zlepšení. Podstatou je posílení vnějšího svěrače a zabránění jeho dalšího poškození. Pacienti se učí relaxovat svěrač během defekace a celkově „trénují“ její správný průběh.
3. Zlatým standardem léčby fekální inkontinence s izolovaným defektem svěrače je overlaping sfinkteroplastika. Disekce vnějšího svěrače s jizvou i jakékoliv identifikovatelné části vnitřního svěrače od okolního tuku a pojiva je následována překrytím a snahou o rekonstrukci prstence svěrače. Z dlouhodobé úspěšnosti dochází během pěti let k selhání operace v polovině případů. Horší výsledek má výkon u pacientů s prodloužením PNTML.
4. Sakrální neuromodulace je ideální pro pacienty se slabým, ale jinak plně funkčním análním svěračem. Podstatou je stimulace sakrálních nervů, při které se nervový stimulátor dočasně umístí na úroveň S3. Pokud dojde následně ke zlepšení alespoň o 50 %, je dočasný stimulátor vyměněn za permanentní, který je implantován subkutánně. Metoda má slibné výsledky se zlepšením stavu u téměř 80 % pacientů.
5. Umělý střevní svěrač je složen z manžety s rezervoáru, který umožní ruční nafouknutí manžety umístěné okolo anu a zvyšující jeho tonus. To umožňuje pacientovi uzavřít anální otvor a při potřebě defekace jej zase povolit. Výkon se provádí pouze vzácně, nevýhodou metody je častý vznik infekčních komplikací (až u 30 % pacientů).
6. Několik let je již k dispozici možnost injekční aplikace kolagenu do sliznice anu, u více než 50 % pacientů bylo dosaženo zlepšení inkontinence o více než 50 % a tento výsledek přetrval déle než roky.
7. Magnetický prstenec Fénix, který je implantován okolo svěračů.
8. V současnosti se testuje užití kmenových buněk ke zvětšení hmoty svaloviny svěračů. Kmenové buňky jsou odebrány z pacientovy svaloviny a po jejich dozrání in vitro jsou inokulovány do oblasti análního svěrače. Dlouhodobější výsledky nejsou zatím k dispozici.
Hemoroidy
Epidemiologie – symptomatické hemoroidy postihují ročně více než 1 milión obyvatel Západu, nezávisle na pohlaví nebo věku (věk je ale považován za rizikový faktor). V rozvojových zemích je prevalence nižší.
Etiologie – rizikovými faktory jsou vyšší věk, dieta s nízkým obsahem vlákniny a vysokým obsahem tuku a následným vznikem zácpy.
Anatomie a patofyziologie – hemoroidální pleteň je normálním součástí análního kanálu a pomáhá v prevenci poškození svěrače. Skládá se ze třech hlavních komplexů (levého laterálního, pravého předního a pravého zadního). Pokud v nich dochází k městnání, mohou začít prolabovat do lumen análního kanálu s postupným oslabením jejich podpůrného systému a progresí prolapsu i ven za análního kanálu, kde jsou náchylné k poranění.
Klasifikace
- vnější hemoroidy – pod úrovní linea dentata, kryty skvamózním epitelem a jsou bolestivé pokud ztrombotizují.
- vnitřní hemoroidy – nad linea dentata, kryté sliznicí nebo přechodným epitelem a představují většinu hemoroidů.
Klasifikace hemoroidů je založena na jejich úrovni protruze a reponibilitě:
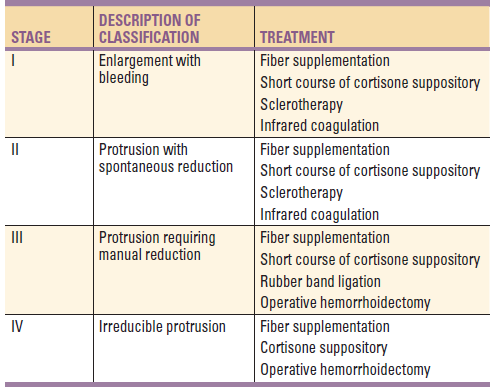
Klinický obraz – pacienti obvykle přichází k lékaři z důvodu:
- Krvácení – většinou nebolestivé, jasně červené krev bývá v toaletě nebo ulpívá na toaletním papíru. Občas může být tak silné, že způsobí až anemizaci pacienta (vždy je třeba vyloučit i maligní příčinu, např. kolorektální karcinom).
- Hmatná protruze – pacienti si stěžují na nemožnost udržení perianální hygieny a často chtějí vyloučit přítomnost malignity.
- Bolest je vzácnější než u fisur a při zvětšování hmoty hemoroidální pleteně bývá spíše tupá. Silná bolest může značit trombózu hemoroidu.
Diagnostika – většinou postačuje fyzikální vyšetření včetně vyšetření per rectum s posouzením přítomnosti trombózy uzlu nebo exkoriace. S ohledem na povahu choroby lze opatrně provést anoskopii při Valsalvově manévru a tím maximální protruzi hemoroidu.
CAVE Vždy je třeba odlišit od prolapsu rekta.
Terapie
1. Léčba krvácejícího pacienta – při krvácení z hemoroidu je třeba vždy vyloučit ostatní příčiny. U mladého pacienta bez rodinné nebo osobní anamnézy kolorektálního karcinomu je možné nejdříve zaléčit hemoroid a kolonoskopii provést až pokud by krev ve stolici neustávala. U starších pacientů je vždy potřeba provést kolonoskopii nebo alespoň sigmoideoskopii k vyloučení malignity. Po vyloučení ostatních příčin lze krvácející hemoroid ošetřit:
- ligací se založením kroužku okolo uzlu s jeho následnou ischemií a trombózou. Tomu pomůže fixace kroužku v análním kanále proximálně od uzlu. Pacienti si během 24 hodin mohou stěžovat na tupou bolest v místě ligace.
- skleroterapií, při které se do podslizničního vaziva uzlu injikuje 1 – 2 ml sklerozující látky (většinou sodná sůl tetradecylsulfátu).
CAVE Pro riziko stenózy anu je třeba se vyvarovat injekce po jeho celém obvodu.
Citlivost tkáně rekta začíná až pod linea dentata, proto lze obě procedury provést ambulantně. Pokud se provádí emergentní hemoroidektomie silně krvácejícího varixu, je nutné počítat s vyšší četností pooperačních komplikací.
2. Léčba trombotizovaného hemoroidu – trombotizovaný hemoroid by měl být do 3 dnů vyříznut eliptickou excizí. Podpůrnou léčbou jsou sedací koupele, změkčení stolice a vláknina.
3. Chirurgická terapie – k chirurgickému ošetření lze provést následující procedury, které jsou v léčbě hemoroidů III – IV. stupně stejně efektivní:
- excizní hemoroidektomie, jejíž výhodou je současné odstranění nadbytečného podkožního vaziva, které jinak tvoří nepěkné řasy prolabující ven z anu.
- THD (transhemoroidální dearterializace), při které je za navigace ultrazvuku identifikována přívodná krevní céva, která je následně ligována s následným zmenšením hemoroidálního plexu.
- hemoroidektomie staplerem, je spojena s menším dyskomfortem pacienta, nevýhodou je ponechání kožních řas
Kontraindikací všech výkonů je přítomnost imunosuprese nebo aktivní proktitidy.
Komplikace terapie hemoroidů
- akutní komplikace – bolest, infekce, recidiva krvácení a močová retence
- chronické komplikace
- inkontinence stolice při iatrogenním poškození svěrače
- stenóza anu při nadměrné excizi tkáně nebo sklerotizaci celého obvodu anu
- ectropion (prolaps rektální sliznice z anu), při kterém si pacienti stěžují na „vlhký“ anus, kdy při prolapsu sliznice nejsou schopni zabránit jeho znečištění.
Anorektální abscesy
Epidemiologie – u mužů 3x častější než u žen, nejčastěji mezi 20 – 40 roky života. Incidence není jasná, anorektální absces je příčinou u 15 % pacientů, kteří pro perianální bolest navštíví chirurga.
Etiologie – nejčastější u pacientů s postiženou imunitou (imunosupresivní léčba, HIV, diabetes mellitus, hematologické malignity) a IBD. Při recidivující perianální infekci by se na tyto příčiny mělo pomyslet.
Anatomie a patofyziologie – anorektální abscesy vznikají infekcí žláz v okolí análního kanálu, které za normálních okolností vytváří hlen napomáhající defekaci. Při náhodném vniknutí stolice do ústí žlázky dojde její infekci a vzniku abscesu.
Klasifikace – dle lokalizace perianální (40 – 50 %), ischiorektální (20 – 25 %), intersfinkterické (2 – 5 %) a supraelevátorské (2,5 %).
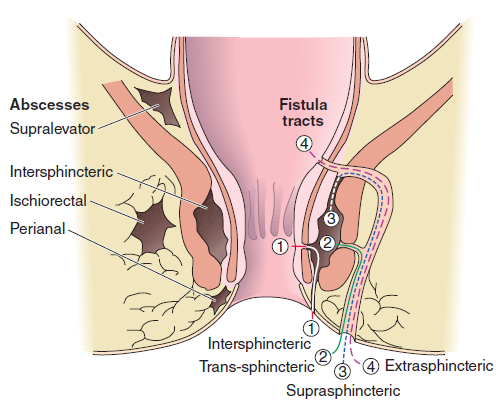
Klinický obraz a diagnostika – hlavními příznaky jsou perianální bolest a horečka. Pacienti popisují obtížné vyprázdnění s přítomností krve ve stolici. Při klinické vyšetření lze prokázat rozsáhlou rezistenci s flukuací, která je často viditelná.
Při laboratorním vyšetření jsou zvýšené markery zánětu, zobrazovací metody jsou jen zřídka potřebné (mimo došetření příčiny recidivujících abscesů, CT a MRI mají 80 % senzitivitu v průkazu nekompletní terapeutické drenáže).
Diferenciální diagnostika
- prostatický absces – podobné příznaky + dysurie. Pacienti mají často v anamnéze sexuálně přenosnou chorobu.
- IBD – při chirurgickém ošetření abscesu je vhodné screeningové provedení sigmoideoskopie k vyloučení IBD. Při podezření na Crohnovu chorobu je třeba doplnit kompletní kolonoskopii + vyšetření tenkého střeva.
Terapie – základem léčby je chirurgická incize a drenáž. Při nekomplikovaném abscesu lze výkon provést ambulantně, u diabetiků nebo imunosuprimovaných osob na operačním sále (vyšší riziko vzniku nekrotizující fascitidy). Dostatečná clona antibiotik je doporučována u imunosuprimovaných pacientů, osob s umělou chlopní, po TEP, diabetiků a s IBD.
Anální píštěl
Epidemiologie – incidence ≈ 1 : 10 000.
Etiologie – souvisí s perianálním abscesem (do píštěle progreduje 30 – 40 % abscesů). Z 90 % je původ kryptoglandulární, ale v 10 % má souvislost s IBD, TBC, malignitou nebo ozářením.
Anatomie a patofyziologie – anální píštěl je definována jako komunikace mezi abscesovou dutinou a análním kanálem, nejčastěji v oblasti linea dentata, protože zde anální žlázky ústí do anu.
Klasifikace – píštěle se dělí podle jejich vztahu k análnímu svěrači na intersfinkterické (70 %), transsfinkterické (23 %), suprasfinkterické (5 %) a extrasfinkterické (2 %).
Klinický obraz – pacienti udávají přetrvávající sekreci z perianální oblasti spojenou s tuhou masou. Tato sekrece může narůstat při defekaci. Je těžké udržet přijatelnou perianální hygienu.
Diagnostika – nejlepším způsobem diagnostiky je fyzikální vyšetření popřípadě anoskopie v celkové anestezii. K ozřejmění ústí píštěle lze využít peroxid vodíku (šumění v místě ústí) nebo MRI (úspěšné v 80 %). Po drenáži je cestou drénu možné provedení retrográdní fistulografie k ozřejmění slepých ramen píštěle.
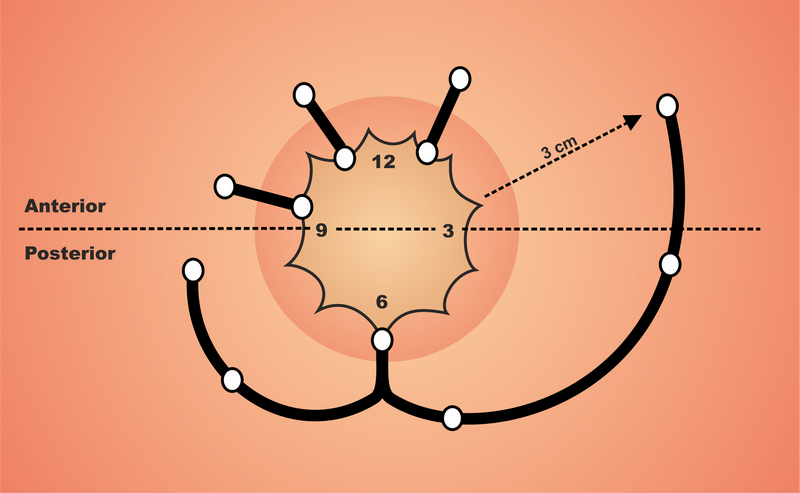
Goodsallovo pravidlo – ozřejmuje ústí jednotlivých druhů píštěle. Pokud je zevní ústí nad příčnou čárou probíhající anem (linea canalis analis transversalis) ventrálně, vnitřní ústí se nachází radiálně na stejném paprsku. Pokud je zevní ústí dorzálně od příčné čáry, vnitřní ústí se nachází ve střední čáře vzadu (u č. 6 podle hodinek). Píštěle ústící ˃ 3 cm od anu mohou toto pravidlo obcházet.
Terapie – většinou chirurgická – nově diagnostikovanou píštěl je vhodné ošetřit tak, aby píštěl zůstala otevřená (uložení ligatury, drénu apod.) a mohla se postupně zklidnit (při jejím uzávěru by opět vzplál zánět). Po zklidnění zánětu je několik způsobů dalšího postupu:
- prostá fistulotomie je vhodná u intersfinkterických a nižších (méně než 1/3 svaloviny) transsfinkterických píštělí (recidiva 0 – 18 %).
- posuvný lalok (advancement flap) spolu s drenáží nebo tkáňovým lepidlem je vhodný u vyšších transsfinkterických píštělí (recidiva 20 – 30 %). U velmi dlouhých (˃ 2 cm) a úzkých píštělí je tkáňové lepidlo vhodnější než u kratších píštělí.
- LIFT (ligation of the internal fistula tract), jednoduchá ligace, má u prostých píštělí také dobrý efekt (recidiva 20 – 30 %).
Režimová opatření po chirurgickém výkonu – pacienti by měli užívat látky změkčující stolici a provádět sedací koupele.
Komplikace chirurgické terapie
- časné – retence moči a krvácení
- pozdní (˂ 10 %) – dočasná nebo trvalá inkontinence
Anální fisura
Epidemiologie – nejčastěji ve věku 20 – 40 let (je nejčastější příčinou krvácení z rekta u dospívajících), u obou pohlaví stejně.
Etiologie – rizikové faktory jsou zácpa/průjem, infekce, perianální poranění nebo Crohnova choroba.
Anatomie a patofyziologie – poranění análního kanálu vzniká obvykle během defekace (v oblasti dorzální poloviny anu), nejčastěji následkem zvýšeného klidového tonu vnitřního svěrače. Krevní cévy zásobující svěrač i sliznici anu vstupují na číslech 3 a 9, místa vzniku fisury (6 a 12) jsou proto nejvíce náchylná k ischemii, která vzniká právě při zvýšeném tonu vnitřního svěrače. Jakékoliv poranění v této oblasti se tak i nejhůře hojí.
CAVE Přítomnost fisury v jiné pozici než na 6. a 12. hodině musí vzbudit podezření, že fisura je sekundárním projevem jiné choroby (viz výše), po které je třeba cíleně pátrat.
Klinický obraz a diagnostika – anální fisuru lze téměř s jistotou diagnostikovat již z důkladného odběru anamnézy. Pacienti si stěžují na perianální bolest, která je silně spojena s defekací (zejména tuhé stolice). Přítomnost krve ve stolici nebývá tak časté, jako při hemoroidech. Při fyzikálním vyšetřením se fisura prokazuje nejčastěji na pozici 6 a 12.
Při chronické fisuře (delší než 6 měsíců) lze nalézt hypertrofickou anální papilu na proximálním pólu fisury s kožním nadbytkem na jejím distálním pólu, na bázi fisury jsou často vidět i cirkulární vlákna hypertrofického vnitřního svěrače (chronicky hypertonický).
Pokud je doplněna i manometrie, je patognomonickým nálezem zvýšený klidový tlak a pilovitá deformace křivky vnitřního svěrače jeho díky paradoxním kontrakcím.
Terapie – léčba akutní fisury je konzervativní, se snahou o změkčení stolice při zácpě, zvýšení dietní vlákniny, aplikací lokálních anestetik, glukokortikoidů a sedacích koupelí. Úspěšnost zklidnění akutní fisury při tomto způsobu je 60 – 90 %.
Při chronické fisuře je snaha o snížení klidového tonu análního svěrače (nifedipin nebo nitroglycerin v masti 3x denně nebo botulotoxin aplikovaný do análního svěrače). Chirurgicky lze provést dilataci anu a laterální sfinkterotomii vnitřního svěrače s protětím cca 1/3 vláken vnitřního svěrače (lze je snadno identifikovat, protože jsou hypertrofická).
Prognóza – úspěšnost farmakoterapie je nižší, při chirurgické terapii je vyšší riziko inkontinence (nejčastěji při sfinkterotomii, častěji u žen).