Anamnéza a fyzikální vyšetření ledvin
Pečlivá a podrobná anamnéza a vyšetření nemocného jsou nejdůležitější součástí diagnostického procesu. V rodinné anamnéze je třeba pátrat po dědičném onemocnění ledvin (zejména polycystické ledviny) a urolitiáze. V osobní anamnéze pak po vrozených anomáliích močového ústrojí (zejména vezikoureterálním refluxu), akutním selhaní ledvin (jakékoliv příčiny a kdykoliv během života) nebo obstrukci močových
cest. Dále je nutné pátrat po chorobách, do jejichž obrazu patří nefropatie (diabetes mellitus – DM, hypertenze, chronické selhání srdce, chronický zánět), ve farmakologické anamnéze po užívání nefrotoxické medikace (diuretika, nesteroidní antirevmatika – NSAID, analgetika, nedávné užití jodové kontrastní látky). Riziková je i přítomnost jedné funkční ledviny. Fyzikální vyšetření má poměrně nízkou senzitivitu i specificitu a normální nález nevylučuje těžké postižení ledvin, přesto je jeho pečlivé provedení vždy nutné. Častá je bledost kůže a sliznic pro současnou anemii, uremické zbarvení kůže je až pozdním příznakem, který se často objevuje až ve fázi hemodialýzy. Dalším znakem jsou otoky při hypervolemii a/nebo hypoalbuminemii, které ale mají i řadu nerenálních příčin. Velmi častá je hypertenze. Vysokou senzitivitu i specificitu má přítomnost krve a bílkoviny v moči. Jednotlivé fáze fyzikálního vyšetření:
- Pohled – normální ledviny nejsou pouhým pohledem viditelné. Vyklenutí pod žeberním obloukem podmíněné zvětšenými ledvinami je vždy patologické (nejčastěji při polycystických ledvinách, pokročilém tumoru ledviny nebo hydronefróze). Suprapubické vyklenutí může způsobit naplněný močový měchýř při hypertrofii nebo nádoru prostaty nebo při nádoru malé pánve.
- Poslech – při stenóze renální tepny může být slyšitelný systolický šelest v oblasti epigastria.
- Poklep – tapottement je šetrný poklep malíkovou hranou v lumbální oblasti bilaterálně. Při pozitivitě (nejčastěji z důvodu akutní pyelonefritidy) vzniká bolestivost v oblasti ledviny
- Pohmat – bimanuální palpace ledvin (Israeliho hmat) – pacient leží na zádech s pokrčenými končetinami v kolenou. Při vyšetření pravé ledviny stojí vyšetřující vpravo u lůžka, levou rukou vyšetřovanou ledvinu tlakem na bederní krajinu „nadzvedává“ proti palpující ruce pravé ruky. U vyšetření levé ledviny je postup opačný.
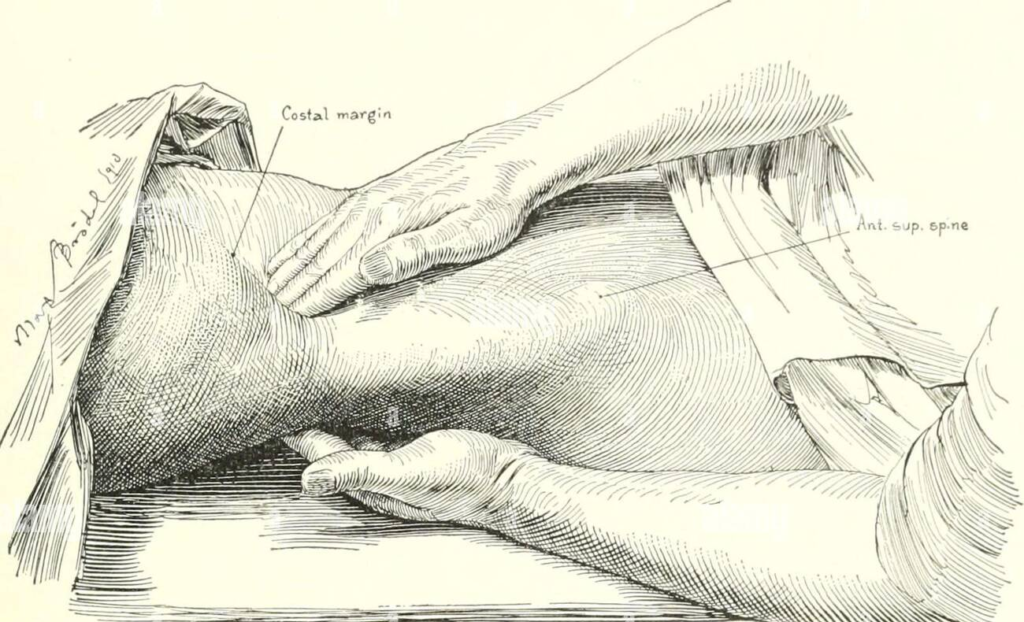
Dále je důležitá palpace ureterálních bodů, kdy pohmatem vyšetřujeme v průsečíku medioklavikulární a umbilikální čáry. Jejich bolestivost se objevuje při ureterolitiáze nebo zánětu.

Jednotlivé názvy močových příznaků a syndromů:
- anurie – vyloučení méně než 100ml moči za den
- oligurie – vyloučení méně než 400ml moči za den
- polyurie – vyloučení více než 2500ml moči za den
- dysurie – obtížné, nepříjemné močení
- polakisurie – opakovaná evakuace malého objemu moči v krátkých
časových intervalech - nykturie – stížnost na probuzení ze spánku kvůli tomu, že pacient
musí jít močit - strangurie – bolest a řezavý pocit při močení
- nefritický syndrom – hematurie, oligurie s azotemií, hypertenze, maximálně středně významná proteinurie. Bývá spojen nejčastějis akutní glomerulonefritidou nebo IgA nefropatií.
- nefrotický syndrom – závažná porucha glomerulární bazální membrány, se zvýšením odpadu bílkoviny močí. Typická je proteinurie s následnou hypoproteinemií, hypoalbuminemií, hypercholesterolemií a otoky.
Anatomie ledvin
Ledviny jsou párový orgán (11–14 cm dlouhý, 5–6 cm široký a 3–4cm silný) nalézající se v retroperitoneu (v úrovni Th12–L3, pravá leží o něco níže než levá z důvodu naléhání jater). V jejich hilu do ledvin
vstupuje renální tepna a vystupuje renální žíla. Jsou obaleny tenkým vazivovým pouzdrem (kapsulou) a obsahují vnější kůru (nachází se zde glomeruly) a vnitřní dřeň. Anatomickou jednotkou ledvin je nefron. U dospělých jedinců obsahuje každá ledvina cca 1 milion nefronů, na druhou stranu u nedonošených vzniká v každé ledvině pouze cca 225 tisíc nefronů, což zvyšuje jejich náchylnost k nefropatiím v dospělosti. Nefron se skládá z klubíčka kapilár (glomerulus), z něj odstupuje tubulus, kde je dále upravována
primární moč. Tubulus se dělí na proximální tubulus, Henleovu kličku, distální tubulus a sběrné kanálky. Nefrony uložené ve vnější části kůry (kortikální nefrony) mají krátké Henleovy kličky, zatímco juxtamedulární nefrony (cca 15% všech nefronů) mají dlouhé Henleovy kličky sahající až k pyramidám. Do glomerulu vstupuje aferentní arteriola a vystupuje z něj eferentní arteriola, jejich endotel je kryt speciálním epitelem a dohromady vytváří Bowmanovo pouzdro, mezi endotelem a epitelem je bazální membrána. Prostor mezi kapilárami glomerulu se nazývá mesangium, zde se nacházejí makrofágy, které mohou po stimulaci produkovat různé cytokiny, např. transforming growth-factor-b (TGF-b). Mesangiální buňky jsou kontraktilní a tím významně regulují glomerulární filtraci (GF). Mezi endotelem a tubulární tekutinou existuje bariéra složená celkem ze tří vrstev. Na krevní straně této bariéry jsou endotelie, který jsou fenestrované s póry cca 70–90 nm velkými (pokryté negativně nabitými glykoproteiny a glykosaminoglykany, tudíž brání prostupu negativně nabitých proteinů, zejména albuminu), následuje bazální membrána a epiteliální vrstva složená z podocytů. Podocyty jsou speciální buňky, které mají řadu různě proplétajících se výběžků (pseudopodia), mezi kterými jsou cca 25 nm velké štěrbiny. Tlusté ascendentní raménko Henleovy kličky se dotýká glomerulu „svého“ nefronu. Tato část tubulu je histologicky modifikovaná a nazývá se macula densa (tvoří se zde renin). Inervace renálních tepen – sympatická pregangliová inervace pochází z dolních hrudních (Th) a horních bederních (L) míšních segmentů, postgangliové neurony se nachází v ganglion mesentericum superior a podél renální tepny. Senzitivní aferentní vlákna sledují sympatické eferentní nervy a vstupují do míchy v Th a horních L kořenech.
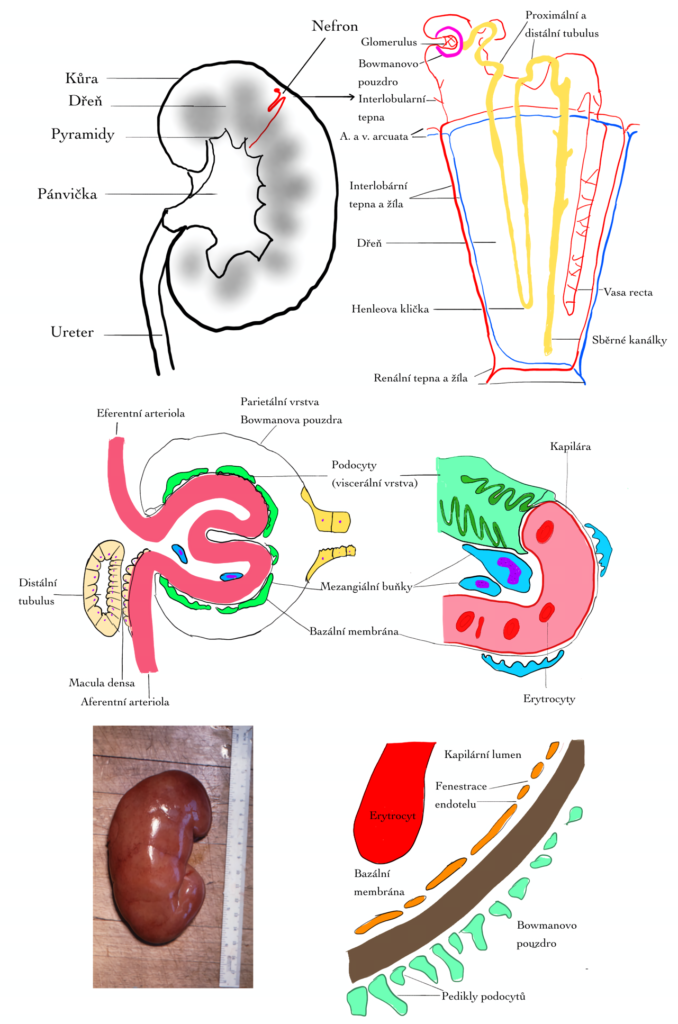
nahoře vpravo: schéma nefronu, uprostřed vlevo: schéma glomerulu, uprostřed vpravo:
bariéra endotel – Bowmanovo pouzdro, dole vpravo detail bariéry endotel – Bowmanovo
pouzdro, dole vlevo: fotografie ledviny.
Fyziologie ledviny
1. Krevní cirkulace
Ledvinami protéká 20 % srdečního výdeje. A. renalis se rozděluje na segmentální arterie, ty se dělí na interlobární arterie, dále na aa. arcuatae a interlobulární arterioly. Aferentní arterioly jsou krátké rovné větévky interlobulárních arteriol, které se dělí na kapiláry tvořící glomerulus (je zde vysoký tlak daný přítomnosti aorty, cca 60 mm Hg) a ty se slévají ve vas efferens, které se opět rozpadají, opřádají tubuly (peritubulární kapiláry, je zde nízký tlak cca 8 mm Hg) a poté vtékají do interlobulárních žil. Nefron má tedy dvě kapilární sítě, které jsou odděleny eferentní arteriolou. Distální kapiláry poté přechází ve venuly, které se sbírají v renální žílu. Kapiláry zásobující tubuly kortikálních nefronů vytváří pouze peritubulární síť, zatímco v případě juxtaglomerulárních glomerulů vytváří mimo peritubulární síť i kličkovité cévy (vasa recta). Ty se zanořují do dřeně, provázejí Henleovu kličku a jsou odpovědné za protiproudový mechanismus. Descendentní část vasa recta má nefenestrovanou výstelku obsahující přenašeč pro ureu, zatímco ascendentní část má fenestrovaný endotel a vstřebává se tudy voda. Kůrou protéká 90 % a dření 10 % z celkového objemu krve a parciální tlak kyslíku klesá od kůry směrem ke dření, která je tak nejvíce citlivá k ischémii.
Celkové množství krve protékající ledvinou se označuje jako glomerulární filtrace (GF) a slouží jako základní kritérium posouzení funkce ledvin. Normální hodnota GF je > 1,5 ml/s. Podél cesty k eferentní arteriole dochází k filtraci velké části vody a filtrovatelných molekul, zvyšuje se koncentrace albuminu (díky negativnímu náboji není filtrován), roste onkotický tlak a filtrace z kapiláry klesá až se zastavuje. Hlavní hnací silou GF je hydrostatický tlak v glomerulu (PGC), proti kterému působí hydrostatický tlak v Bowmanově pouzdře (PBP) a onkotický tlak v glomerulu (píGC), který vzniká přítomností nefiltrovatelných plasmatických proteinů, zejména albuminu a snaží se udržet tekutinu uvnitř glomerulární kapiláry. GF je tak ovlivňována zejména hodnotou PGC. Základní vlastností renální cirkulace je autoregulace, která zajišťuje stabilní krevní průtok ledvinou v širokém rozmezí středního arteriálního tlaku (MAP) 65 – 180 mm Hg. Tato autoregulace je zajištěna následujícími mechanismy:
- myogenní reflex – akutní změny v perfúzním tlaku ledvin působí konstrikci nebo dilataci aferentní tepny (zvýšení tlaku konstrikci, snížení dilataci).
- tubuloglomerulární feedback – oblast macula densa ve vzestupném raménku Henleovy kličky „analyzuje“ rychlost toku v tubulární tekutině, která je vyjádřena jako koncentrace Na+. Při jejím zvýšení se zvyšuje i štěpení ATP při aktivním tubulárním transportu za vzniku adenosinu, který je silným vasokonstriktorem aferentní arterioly, což zase sníží GF. Mechanismus samozřejmě funguje i obráceně (snížená koncentrace adenosinu vede k poklesu TK a vasodilataci aferentní arterioly).
- renin – angiotenzin – aldosteronový systém (RAAS) – viz níže.
GF se stanoví několika způsoby:
1/ Pomocí látek, které jsou volně filtrované glomeruly a nejsou vylučovány, ani resorbovány v tubulech. GF se určí jako poměr koncentrace této látky v moči (U) a plazmě (P), vynásobený celkovým množstvím moči (V): GF = (U/P) . V
Touto látkou je např. polymer fruktózy inulin, ale jelikož je v praxi takovéto stanovení velice složité (nutnost intravenózního podání, udržení standardní hladiny pomocí trvalé infúze, odběr vzorku arteriální krve, vzorku moče a stanovení hladiny inulinu) používají se jiné látky. Kreatinin je cyklický amid kreatinu, který vzniká ve svalech a jeho plasmatická hladina je přímo úměrná množství svalové hmoty (je obvykle vyšší u mužů než u žen). Oproti inulinu se částečně vylučuje i tubulární sekrecí, ale tato nepřesnost je v klinické praxi zanedbatelná (zvyšuje se při pokročilejším renálním selhání, kdy poměr části vylučované tubuly stoupá) a dále má sníženou citlivost v časných fázích glomerulární dysfunkce (GF 1,0 – 1,5 ml/s). Hladina clearance kreatininu lze určit více způsoby:
- nejpřesnější je 24hodinový sběr moči se stanovením jejího celkového množství a koncentrace kreatininu v plazmě a moči. Vzhledem k pracnosti lze GF spočítat i jinak:
- dle Cockrofta – Gaulta, vzorec je již považován za obsolentní (online kalkulátor: https://www.mdcalc.com/calc/43/creatinine-clearance-cockcroft-gault-equation).
- dle MDRD (Modification of Diet in Renal Diseas) – v současnosti doporučen Českou nefrologickou společností (online kalkulátor: https://www.mdcalc.com/calc/76/mdrd-gfr-equation), CAVE s výjimkou dětí a těhotných. GF = 515,3832 . Skr-1,154 . věk-0,203 . 0,742 (ženy) . 1,21 (černá populace)
- CKD EPI – v současnosti používán některými laboratořemi (online kalkulátor: https://www.mdcalc.com/calc/3939/ckd-epi-equations-glomerular-filtration-rate-gfr).
GF = 142 . min(Skr/κ, 1)α. max(Skr/κ, 1)-1.200. 0,9938věk . 1,018 (ženy) . 1,159 (černá populace)
kde je Skr …koncentrace sérového kreatininu v mg/dL, κ koeficient…0,7 (ženy) nebo 0,9 (muži), α koeficient… -0,241 (ženy) nebo -0,302 (muži), min(Skr/κ, 1) je minimální hodnota Skr/κ nebo 1.0, max (Skr/κ, 1) je maximální hodnota Skr/κ nebo 1,0, věk v rocích.
CAVE Závislost Skr na GF není lineární, ale hyperbolická. Při zhoršování funkce ledvin tedy plasmatická Skr stoupá pozvolna a dalším zhoršením se vzestup zrychluje.
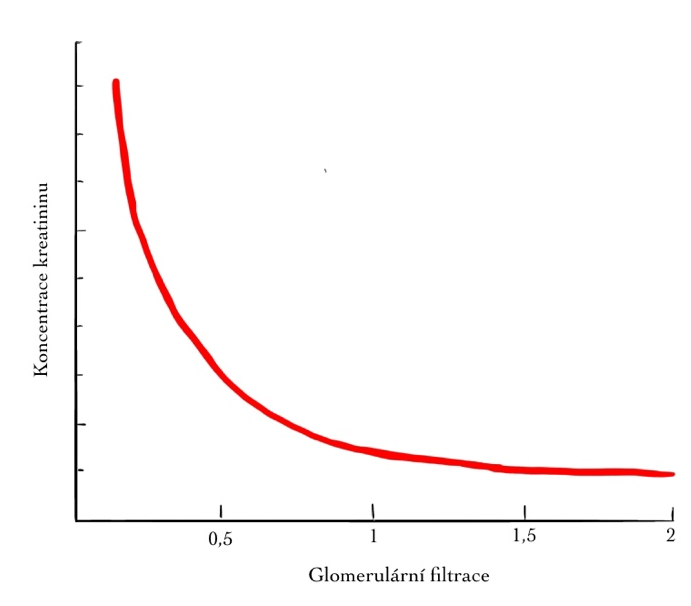
2/ Stanovením hladiny inhibitoru cysteinových proteáz cystatinu C. Tato látka je vytvářena všemi jadernými buňkami, volně prochází glomerulární membránou a je resorbována tubulárními buňkami, kde je metabolizována…tedy, čím více cystatinu C je obsaženo v extracelulární́ tekutině, tím je GF nižší. Pro vypočet GF z koncentrace cystatinu C v séru se používá rovnice dle Grubba: GF = 1,4115 . Scyst -1,680 . F, kde je Scyst … koncentrace cystatinu C v séru v mg/l, F … koeficient (děti do 14 let F = 1,384; muži F = 1; ženy F = 0,948). Vypočet je vhodné používat pro pacienty s GF > 0,3 ml/s.
CAVE GF stanovená cystatinem je falešně snížena při terapii glukokortikoidy a falešně zvýšena hypotyreózou.
3. Izotopové metody vyšetření GF (99mTc–DTPA (diethyltriaminopentaoctová kyselina), 51Cr–EDTA (ethylendiaminotetraoctová kyselina), 125I–thalamát) – radionuklidové metody používané k vyšetření renálních funkcí umožnují́ posoudit vylučování izotopem značených látek z organismu ledvinami. Rychlost poklesu aktivity v plazmě je dána velikostí GF, resp. tubulární́ sekrece. Při dynamické scintigrafii je také́ možnost posoudit odděleně funkci pravé́ a levé́ ledviny.
2. Vylučování vody a solutů, regulace objemu extracelulární tekutiny
Lidské tělo je složeno z 50 % vody u žen a 60 % u mužů. Průměrný normální příjem tekutin je 2100 ml potravou, 200 ml voda produkovaná metabolismem. Výdej tekutiny má více složek: 1400 ml moč, 700 ml perspiratio insensibilis (neměřitelné ztráty) plícemi (350 ml) a kůží (350 ml), 200 ml perspiratio sensibilis potem (100 ml), stolicí (100 ml). Ta je rozdělena do několika kompartmentů:
- Intracelulární tekutina (ICT, 55 – 75 % celkové vody).
- Extracelulární tekutina (ECT, 25 – 45 % celkové vody), ta je rozdělena na intravaskulární (IVT) a intersticiální (IST) vodu v poměru 1:3. Oba tyto kompartmenty jsou odděleny kapilární stěnou a pohyb vody mezi nimi je řízen Starlingovými silami (hydrostatický a onkotický tlak).
Osmolalita
Jako osmolalita se označuje koncentrace částic v tekutině a je vyjadřována v miliosmolech na kilogram vody (mOsm/kg). Voda volně proniká přes plasmatickou membránu se snahou o dosažení osmotické rovnováhy (osmolalita ICT = osmolalita ECT). Soluty většinou přes membrány volně nedifundují, ale využívají různé kanály a transportéry. Hlavními soluty ECT jsou Na+, Cl– a HCO3–, v případě ICT to jsou K+ a organické estery fosfátů (ATP, kreatin fosfát a fosfolipidy). Soluty, které nemohou přes membránu volně procházet a jsou tak „uzavřeny“ v daném kompartmentu vytvářejí efektivní osmolalitu. Jiné soluty (např. urea) se nepodílí na ovlivnění proudění vody přes membránu a označují se tak jako neefektivní soluty. Na udržení normální osmolality 280 – 295 mOsm/kg se podílí antidiuretický hormon, příjem čisté vody a vylučování vody a solutů ledvinami.
Antidiuretický hormon
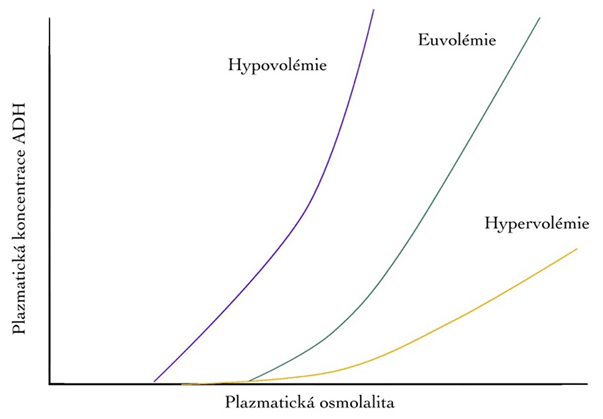
Antidiuretický hormon (ADH, vasopresin) je oligopeptid o 9 aminokyselinách, který je produkován v magnocelulárních neuronech hypotalamu, jejichž distální vlákna končí v neurohypofýze, kde je ADH skladován a odkud je uvolňován do oběhu. Osmoreceptory hypotalamu jsou aktivovány, uvolňují ADH a indukují pocit žízně při zvýšení osmolality krve nad 285 mOsm/kg. Nad touto hranicí je vztah mezi osmolalitou a koncentrací ADH v cirkulaci lineární. Dalším stimulem k uvolnění ADH (slabším než osmolalita) je snížení efektivního cirkulujícího objemu. Výsledkem je, že při hypovolémii dochází k uvolňování ADH již při nižší osmolalitě a křivka koncentrace ADH-osmolalita je strmější. Při hypervolémii dochází k opačné situaci. Organismus umí na změny efektivního cirkulujícího volumu a osmolality rychle reagovat, protože poločas ADH v cirkulaci je pouze 10 – 20 minut. Na základě působení ADH jsou ledviny schopny produkovat vysoce hyperosmolární moč o osmolalitě až 1200 mOsm/l. Naopak, při absenci ADH (diabetes inspidus) je vylučováno velké množství hypoosmolání moči o osmolalitě 50 mOsm/l. K uvolnění ADH vede i řada jiných „neosmotických“ stimulů, např. nauzea, intracerebrální angiotenzin II, serotonin a řada léků.
Hlavním místem účinku ADH je tlustá část vzestupného raménka Henleovy kličky, distální tubulus a hlavní buňky sběracích kanálků, kde se váže na V2 receptory s následnou aktivací cAMP, proteinkinázy A a fosforylací řady transportních proteinů:
- aktivace Na+/Cl– transportéru a K+ kanálu tlusté část vzestupného raménka Henleovy kličky vede k hyperosmolaritě dřeně ledvin, která je základní podmínkou vzniku protiproudového mechanismu. Transport urey dále renální osmotický gradient zvyšuje.
- aktivace akvaporinů 2 a jejich uložení do plasmatické membrány hlavních buněk sběracích kanálků vede ke zvýšení resorpce vody na základě osmotického gradientu (akvaporiny 1 jsou otevřeny trvale).
Natriuretické peptidy
Polypeptidy, které účinkují cestou cGMP a jsou produkovány v srdci, ledvinách a mozku. Mají vasodilatační účinek, zvyšují natriurézu a diurézu, snižují proliferaci buněk i aktivitu sympatiku. Lze rozlišit:
- ANP (atrial natriuretic peptide, 28 aminokyselin), který vzniká ve svalovině srdečních síní a vzniká z preproANP (151 aminokyselin) a proANP (126 aminokyselin).
- BNP (brain natriuretic peptide, 32 aminokyselin) vzniká z prekurzoru preproBNP (134 aminkyselin) a proBNP (109 aminokyselin). BNP spolu s N terminálním peptidem odštěpeným z proBNP slouží jako základní laboratorní markery srdečního selhání.
- CNP (C-type natriuretic peptide)
- urodilatin
RAAS
Renin je syntetizován v granulárních buňkách aferentních arteriol (produkce je regulována beta-1 receptory aferentních arteriol, signály z macula densa, prostaglandiny atd.). Renin štěpí angiontenzinogen na angiotenzin-I, který angiotenzin-konvertující enzym štěpí na angiotenzin-II, který stimuluje:
- ENaC se zvýšením resorpce Na+ ve sběrných kanálcích.
- antiport Na+/H+ se zvýšením resorpce Na+ a exkrece H+.
- sekreci aldosteronu v nadledvinách.
- negativní zpětnou vazbou inhibuje sekreci reninu.
- vasokonstrikci eferentní arterioly se zvýšením intraglomerulárního tlaku a glomerulární filtrace i filtrační frakce. Dochází ke zvýšení peritubulárního onkotického tlaku a snížení tlaku ve vasa recta, což opět zvyšuje resorpci Na+.
Aldosteron
Aldosteron je produkován v zona glomerulosa nadledvin. Váže se na cytoplasmatický mineralokortikoidní receptor hlavních buněk sběrných kanálků, kde zvyšuje aktivitu:
- ENaC
- apikálních kanálů pro K+
- Na+/K+ ATPázy
Dochází tak ke zvýšení resorpce Na+ a nárůstu pozitivního náboje intracelulárně, což vytlačuje K+ do tubulů a zvyšuje tak jeho exkreci.
Udržení objemu ECT
Vzhledem k tomu, že 85 – 90 % všech Na+ iontů se nachází extracelulárně, je množství extracelulární tekutiny (jako jedna z determinant efektivního cirkulujícího volumu) funkcí celkového množství Na+ v organismu. Na+ je filtrován v glomerulech a následně resorbován v ledvinných tubulech, typicky spolu s Cl–, proto se i tento aniont podílí na homeostáze extracelulární tekutiny. Celková hodnota glomerulární filtrace je 180 litrů/den a při natrémii 140 mmol/l tedy ledviny přefiltrují 25200 mmol Na+ denně, z toho se zpět resorbuje 25100 mmol a pouze 100 mmol Na+ (99,6 %) přechází do definitivní moči. Transport Cl– do značné míry odpovídá Na+, protože souhrn všech vstřebaných solutů musí být elektroneutrální. V jednotlivých oddílech nefronu se Na+ resorbuje odlišně, ve všech oddílech je bazocelulárně přítomna Na+/K+ ATPáza:
- 67 % v proximálním tubulu paracelulárně i transcelulárně (v luminální membráně symport s glukózou a aminokyselinami a antiport s H+, bazocelulárně symport s HCO3–).
- 25 % v Henleově kličce paracelulárně i transcelulárně (ve vzestupné části je furosemid senzitivní Na+/K+/2Cl– symport a antiport s H+, bazocelulárně i antiport Cl–/HCO3–).
- 5 % v distálním tubulu transcelulárně (v luminální membráně je Na+/Cl– symport citlivý na thiazidy).
- 3 % ve sběracím kanálku transcelulárně (v luminální membráně je epitelový kanál ENaC citlivý na amilorid). Cl– jsou resorbovány ve vmezeřených buňkách na luminální membráně přes antiporty Cl–/HCO3– a Cl–/OH–.
Regulace tubulární resorpcí Na+ a Cl–:
- v proximálním tubulu ji zvyšuje angiotenzin II a sympatikus, snižuje dopamin.
- v distálním tubulu ji zvyšuje aldosteron (aktivace ENaC hlavních buněk → zvýšení sekrece K+).
Zachování dostatečné volémie je zásadní pro zachování perfúze životně důležitých orgánů. Funkce krevního objemu je dána vaskulární rezistencí, srdečním výdejem, tepovou frekvencí a množstvím vody a extracelulárních solutů, z nichž je nejdůležitější Na+. Za normálních podmínek je volum regulován právě množstvím (nikoliv koncentrací!!!) Na+.
Při hypovolémii se aktivují volumo- a baroreceptory, což vede k neurohumorální aktivaci – sympatiku, RAAS, ADH. Následkem je synergické zvýšení resorpce Na+, Cl– i vody a nárůst vaskulární rezistence. Podobná situace se děje i při poklesu srdečního výdeje při srdečním selhání, hypovolémii, snížení onkotického tlaku, zvýšení kapilární permeability nebo excesivní vasodilataci.
3. Tubulární funkce
Na vnitřní straně tubulů je jedna vrstva specifických buněk, které mají specifické transportní funkce a na okrajích jsou s ostatními spojeny pomocí tights junctions. Buňky jsou navíc polarizované, strana směrem do lumen tubulů se nazývá apikální, směrem opačným bazolaterální. Přes tubuly probíhá řada transportních dějů, jednak přes buňku (transcelulárně) a jednak přes tight junctions (paracelulárně). Transcelulárně jsou využívány různé kanály, aktivní transport (užívá energii z ATP) a sekundární aktivní transport (kotransport). Aktivní transport vytváří asymetrickou koncentraci iontů na obou stranách buněčné membrány a může probíhat proti chemickému gradientu.
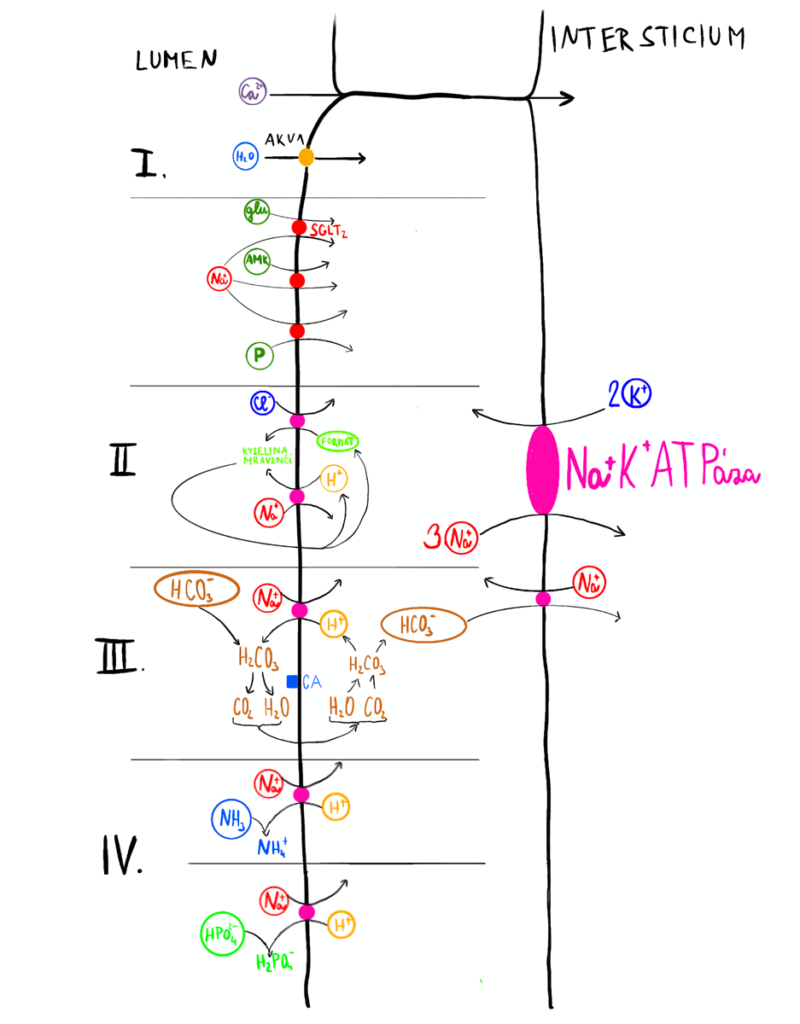
Proximální tubulus
Plocha apikální plochy tubulárních buněk je zvýšena četnými mikroklky. V proximálním tubulu dochází k resorpci cca 2/3 filtrovaného NaCl a vody, až 90 % filtrovaného bikarbonátu a dále téměř všechny molekuly glukózy a aminokyselin. Resorpce vody a iontů je řízena vysokým onkotickým a nízkým hydrostatickým tlakem ve vasa recta (obrazně je zde voda „nasávána“). Buněčný transport většiny solutů (např. aminokyseliny, glukóza, fosfáty) je v proximálním tubulu spřažen s Na+, jehož koncentrace je intracelulárně udržovaná nízká díky aktivitě Na+/K+ ATPázy, která se nachází bazolaterálně. Z deskriptivních důvodů lze tubulární funkce rozdělit na několik oddílů:
- Voda je resorbována trvale aktivními akvaporiny 1, které jsou přítomny na bazolaterální i apikální membráně.
- Chloridy jsou v počátečních segmentech proximálního tubulu špatně resorbovány a vzestup Cl– elektricky vyvažuje pokles HCO3– jak je postupně resorbován v proximálním tubulu. Cl– je transportován antiportem s intracelulárními formáty a bazolaterálně resorbovány pomocí K+/Cl– symportu. Formáty v tubulech přijímají H+ díky Na+/H + antiportu, dochází ke vzniku kyseliny mravenčí, která volně difunduje přes apikální membránu intracelulárně a zde uvolňuje H+, který se tak může být znovu použit.
- V proximálním tubulu je resorbován téměř všechen bikarbonát. Vodíkové ionty se do lumen dostávají téměř výhradně díky Na+/H+ antiportu a téměř ihned se slučují s HCO3– za vzniku H2CO3, která je pomocí enzymu kartáčového lemu karboanhydrázy štěpen na CO2 a H2O. CO2 difunduje do buněk tubulů, kde je opačným dějem tvořen HCO3– a H+. HCO3– je resorbováno pomocí bazolaterálního symportu Na+/HCO3– a H+ je opět vylučováno do tubulární tekutiny pomocí Na+/H+ antiportu.
- V proximálním tubulu dochází k vylučování kyseliny pomocí amoniaku NH3 (vzniká z glutaminu), který příjme H+ za vzniku NH4+ a následně je vyloučen do moči (tvorba amoniaku je mimo jiné nepřímo úměrná kalémii) a HPO42-, na který se váže H+ za vzniku H2PO4–.
- Glukóza je resorbována pouze v proximálním tubulu, transport je apikálně spřažen s Na+ (SGLT2 transportér), na bazolaterální straně poté usnadněnou difúzí. Tento transport je saturovatelný, při glykémii > 10 – 11 mmol/l se cukr objevuje již v moči a dochází ke glykosurii.
- V proximálním tubulu dochází k resorpci 2/3 Ca2+ a cca 85 % anorganického fosforu. Kalcium je resorbováno zejména paracelulárně pasivní difuzí, u fosfátů je transport spřažen s Na+, který je inhibován FGF-23 (fibroblast-growth hormon, vzniká v kostech a snižuje fosfatémii) a dále PTH. V buňkách proximálního tubulu dochází k bioaktivaci 25-OH vitamínu D na 1,25-OH vitamín D, který zvyšuje resorpci kalcia v tenkém střevě (stimulováno PTH).
- V proximální tubulu se resorbují aminokyseliny pomocí několika transportérů (např. cystin, lyzin, arginin a ornitin je resorbován pomocí systému kódovaného geny SLC3A1 a SLC7A9, kdy mutace jednoho z nich je odpovědna za vznik cystinurie).
P glykoprotein má za úkol resorpci a transport několika velice důležitých léků (takrolimus, cyklosporin, digoxin atd.) a má zásadní úlohu v interakcích mezi léky. Přítomny jsou i transportéry pro organické anionty (uráty, dikarboxylové anionty atd.).
Henleova klička
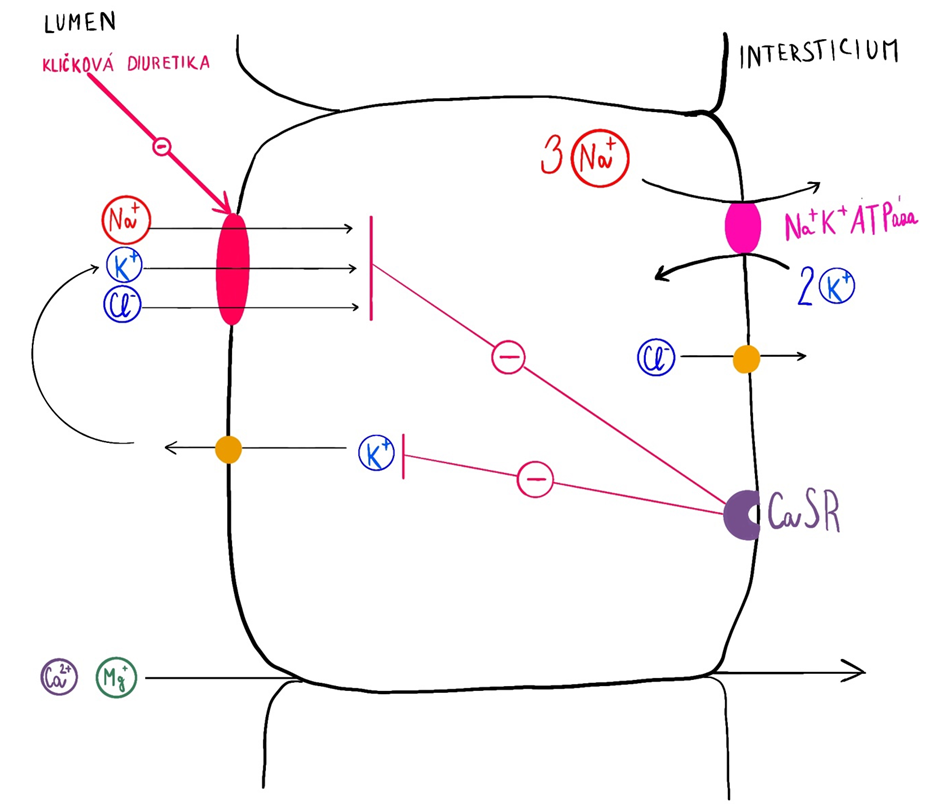
V Henleově kličce je resorbováno cca 15 – 25 % NaCl (zejména v ascendentní tlusté části) a hraje důležitou roli v protiproudovém mechanismu. Henleova klička se skládá z několika segmentů:
- descendentní část je vysoce propustná pro vodu díky trvale aktivním akvaporinům 1.
- ascendentní tenká část je nepropustná pro vodu.
- ascendentní tlustá část je nepropustná pro vodu, ale je vysoká propustnost pro Na+ díky apikálnímu Na+/K+/2Cl– symportu (limitujícím substrátem je tubulární koncentrace K+, který je recyklován apikálním K+ kanálem). Tyto ionty jsou dále bazolaterálně resorbovány díky Na+/K+ ATPáze a Cl– kanálům. Na+/K+/2Cl– symport je blokován kličkovými diuretiky a jeho mutace působí Barterův syndrom (hypokalémie a metabolická alkalóza).
Recyklace K+ se podílí na pozitivním náboji uvnitř tubulu, který podporuje paracelulární resorpci divalentních kationtů (Mg2+ a Ca2+). Definitivní resorpci Ca2+ umožňuje CaSR (calcium sending receptor) v bazolaterální membráně, který může zvýšit kalciurii (hypofunkční mutace CaSR působí familiární hyperkalcemickou hypokalciurii) a zároveň inhibuje Na+/K+/2Cl– symport i apikální K+ kanál.
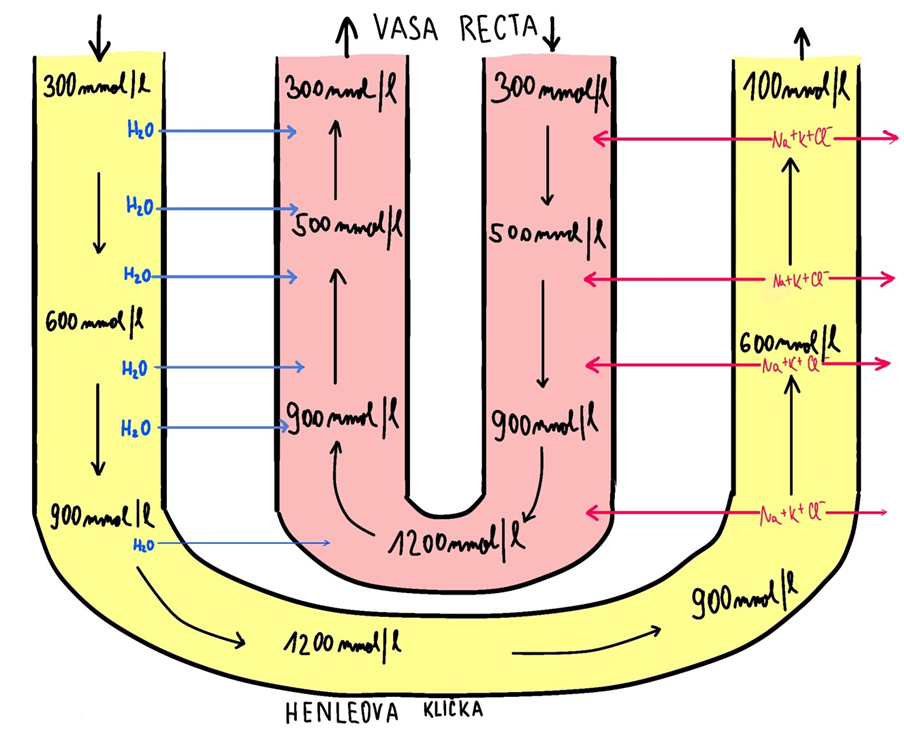
Henleova klička se podílí na vzniku protiproudového systému (zahrnuje Henleovu kličku a vasa recta) a udržení hypertonického intersticia dřeně, a tak na koncentraci moči, protože dochází k excesivní resorpci NaCl (na tomto se podílí i recyklace urey ze sběrných kanálku). Protiproudový systém zahrnuje jednak Henleovu kličku, jednak vasa recta. Na počátku je osmolalita v descendentním i ascendentním raménku cca 300 mosm/l, Na+K+ ATPázy v tlusté části ascendentního raménka navíc pumpují soluty do intersticia (do tubulárních buněk se dostávají zejména cestou Na+/K+/2Cl– symportu) , čímž zde osmolalita dále roste. Voda se pak začíná pohybovat z tenkého descendentního raménka, aby se dostal jeho obsah do osmotické rovnováhy s intersticiem. Z proximálního tubulu sem ale neustále vstupuje tekutina s osmolalitou 300 mosm/l a obsah ředí, takže gradient, proti kterému jsou soluty pumpovány je snižován a více vody vstupuje do intersticia. Tento proces se neustále opakuje a výsledkem je, že od základny kličky k jejímu vrcholu se osmolalita neustále zvyšuje (je tím delší, čím delší je klička). Osmotický gradient ve dřeňových pyramidách dále zvyšuje urea, pro kterou je prostupný pouze tubulární epitel sběrných kanálků…tedy, když moč sestupuje, tak se odstraňuje voda, když vystupuje, tak se odstraňují soluty.
Distální tubulus
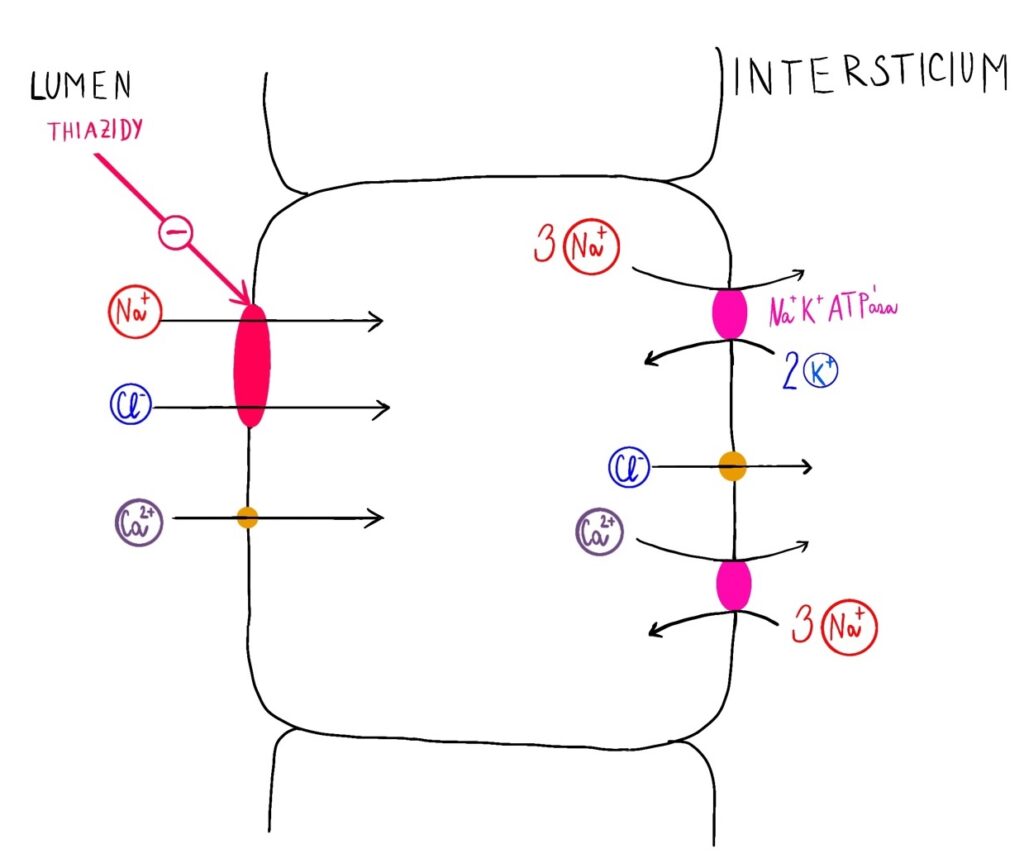
V distálním tubulu je resorbováno 5 % filtrovaného NaCl a je velmi málo prostupný pro vodu:
- hlavním transportérem je apikální Na+/Cl–symport ve spolupráci s Na+/K+ ATPázou a Cl– kanálem bazolaterálně.
- apikálně se nachází Ca2+ selektivní kanály (TRPV5) a bazolaterálně antiport Na+/Ca2+.
Resorpce Ca2+ je nepřímo úměrná resorpci Na+ a je stimulována PTH. Při léčbě thiazidy dochází k blokádě Na+/Cl– symportu, snižuje se množství Na+ intracelulárně, kde je tedy méně kationtů, jejichž místo přebírá Ca2+ a navíc je díky tomu více substrátu pro Na+/Ca2+ antiport. Výsledkem je tedy vyšší resorpce Ca2+.
Pseudohypoaldosteronismus II. typu – mutace genu WNK1 a WNK4 serin-threonin kinázy nebo KLHL3 (Kelch-like 3) a CUL3 (Cullin 3), což jsou dvě komponenty a zároveň regulátory komplexu ubikvitin ligázy E3. Všechny tyto proteiny regulují (v tomto případě zvyšují) funkci Na+/Cl– symportu v distálním tubulu. Klinicky přesný opak Gitelmannova syndromu. Projevuje se hypertenzí, hyperkalémií, hyperchloremickou metabolickou acidózou, supresí PRA a aldosteronu a hyperkalciurií se sníženou kostní denzitou. K hyperkalémii dochází snížením aktivity K+ kanálů ve sběrných kanálcích (není zde dostatek Na+ k resorpci přes ENaC a následnému „elektrickému vytlačení“ K+ do tubulů). Po podání thiazidů dochází k úpravě stavu.
Gitelmanův syndrom – inhibiční mutace genu pro Na+/Cl– symport v distálním tubulu. Projevuje se hypomagnezémií, hypokalciurií (tou se liší od Bartterova syndromu), hypokalémií, hypokalemickou alkalózou, a navíc často chondrokalcinózou (abnormální depozice kalcium pyrofosfát dihydrátu v kloubní chrupavce). Projevy poruchy jsou mírnější než u Bartterova syndromu. Syndrom klinicky odpovídá předávkování thiazidy.
Familiární hypomagnezémie s hypokalcémií – mutace TRPM6, který kóduje kanál pro Mg2+.
Transportní děje ve sběrných kanálcích
Sběrné kanálky modulují konečnou podobu moče, je zde resorbováno cca 4 – 5 % filtrovaného Na+ a jsou důležité pro hormonální regulaci vodní a iontové rovnováhy. Lze je rozdělit na kortikální a dřeňovou část. Veškerý transport zde probíhá transcelulárně. Na apikální části buněk je přítomen akvaporin 2, na bazolaterální akvaporin 3 a 4. ADH se váže na V2 receptory s následnou aktivací cAMP, proteinkinázy A a fosforylací akvaporinů 2, které se následně umisťují na apikální stranu, tvoří zde póry a velmi výrazně zvyšují propustnost membrány pro vodu.
I. Epitel korových sběrných kanálků obsahuje dva typy buněk:
1. Hlavní buňky, které mají úlohu v resorpci vody a Na+ a exkreci K+. Na+ je resorbován přes amilorid senzitivní epitelový kanál (ENaC) a bazolaterálně buňky opouští cestou Na+/K+ ATPázy. Tento proces je úzce regulován aldosteronem, který vstupuje dovnitř buňky z bazolaterální strany, váže se na mineralokortikoidní receptor a ovlivňuje transkripci s následným zvýšením resorpce Na+ a exkrece K+.
Hyperfunkční mutace ENaC vede k Liddleho syndromu se vznikem hypertenze, hypokalémie a metabolické alkalózy. Naopak, amilorid funkci ENaC blokuje.
Resorpcí Na+ dochází ke vzniku pozitivního náboje uvnitř buňky a negativního náboje v lumen tubulů. Dochází tak k přestupu K+ na základě elektrického gradientu do lumen tubulů. Vylučování draslíku je ovlivněno:
- aldosteronem, který zvyšuje aktivitu ENaC i draslíkových kanálů a zvyšuje vylučování K+.
- volumexpanzí nebo diuretiky, které zvyšují tok tubulární tekutiny a zvyšuje se tak i rychlost vylučování K+.
- přítomností neresorbovatelných aniontů v lumen (bikarbonát, peniciliny), které zvyšují elektrický gradient, a tak i vylučování K+.
- některými antibiotiky (trimetoprim, pentamidin), které blokují ENaC a zmenšují tak elektrický gradient se snížením vylučování K+.
2. Vmezeřené buňky zprostředkovávají udržování acidobazické rovnováhy cestou protonové pumpy (H+ATPáza) a Cl–/HCO3– antiportu.
- typ A zprostředkuje exkreci kyselin a resorpci bikarbonátů, kdy protonová pumpa je na apikální membráně a Cl–/HCO3– antiport bazolaterálně. H+ v lumen je následně vázán na NH3 (difunduje do lumen z okolního intersticia) za vzniku NH4+, které je vylučováno močí. Aldosteron zvyšuje počet protonových pump, a tak zvyšuje kyselou exkreci a může působit metabolickou alkalózu.
- typ B zprostředkuje resorpci kyselin a exkreci bikarbonátů), kdy je protonová pumpa bazolaterálně a Cl–/HCO3– antiport apikálně.
Pro zapamatování: buňky typu A, jdou organismem preferovány při Acidémii a protonová pumpa se nachází Apikálně, buňky typu B jsou organismem preferovány při nadbytku Bazí a protonová pumpa se nachází Bazolaterálně.
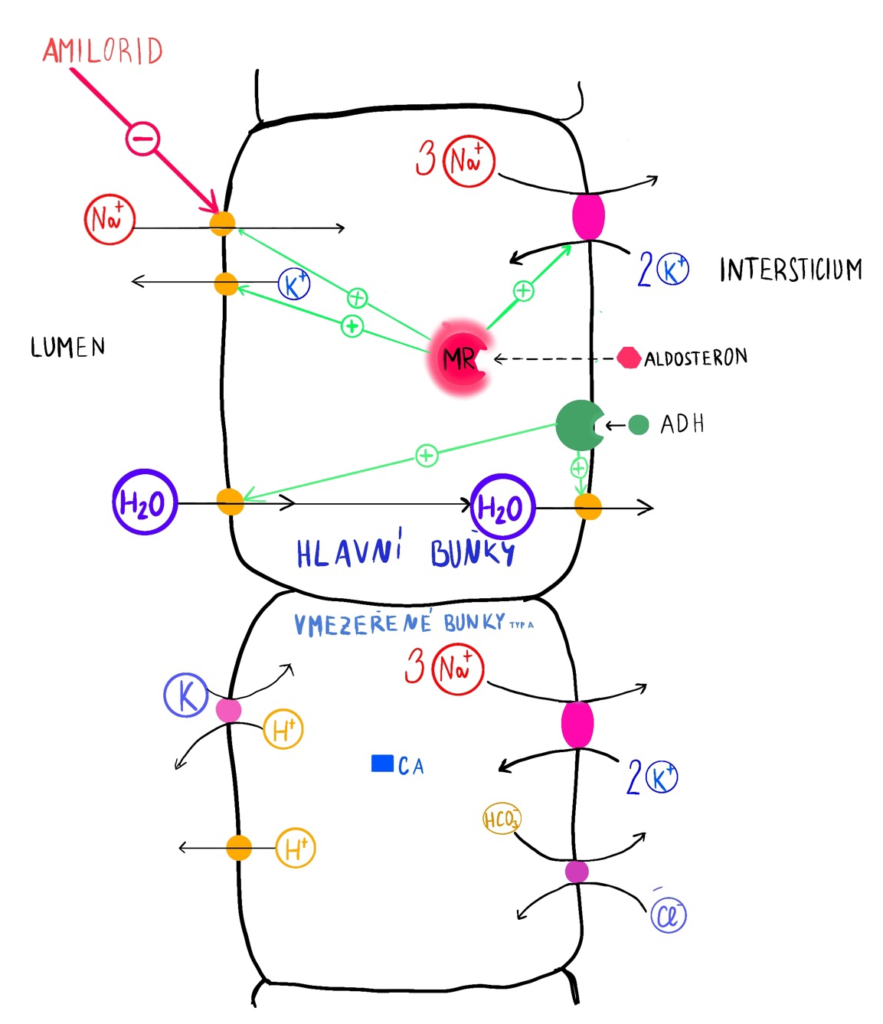
Epitel korových sběrných kanálků obsahuje dva typy buněk (hlavní – nahoře, vmezeřené typu A – dole). CA – karboanhydráza, MR – mineralokortikoidní receptor.
II. Dřeňové sběrné kanálky sdílí mnoho společných znaků s kortikálními kanálky, navíc:
- jsou místem účinku renálních (urodilatin) a atriálních natriuretických peptidů (ANP, uvolňovány z myocytů síní jako odpověď na volumexpanzi). Stimulují guanylyl cyklázu a zvyšují hladinu cGMP se snížením aktivity apikálních Na+ kanálů a zvýšením natriurézy.
- zde dochází k transportu urey mimo lumen, kde se podílí na vzniku hypertonického intersticia, a tak i na protiproudovém mechanismu. Urea se poté dostává zpět do lumen Henleovy kličky pasivní difúzí.
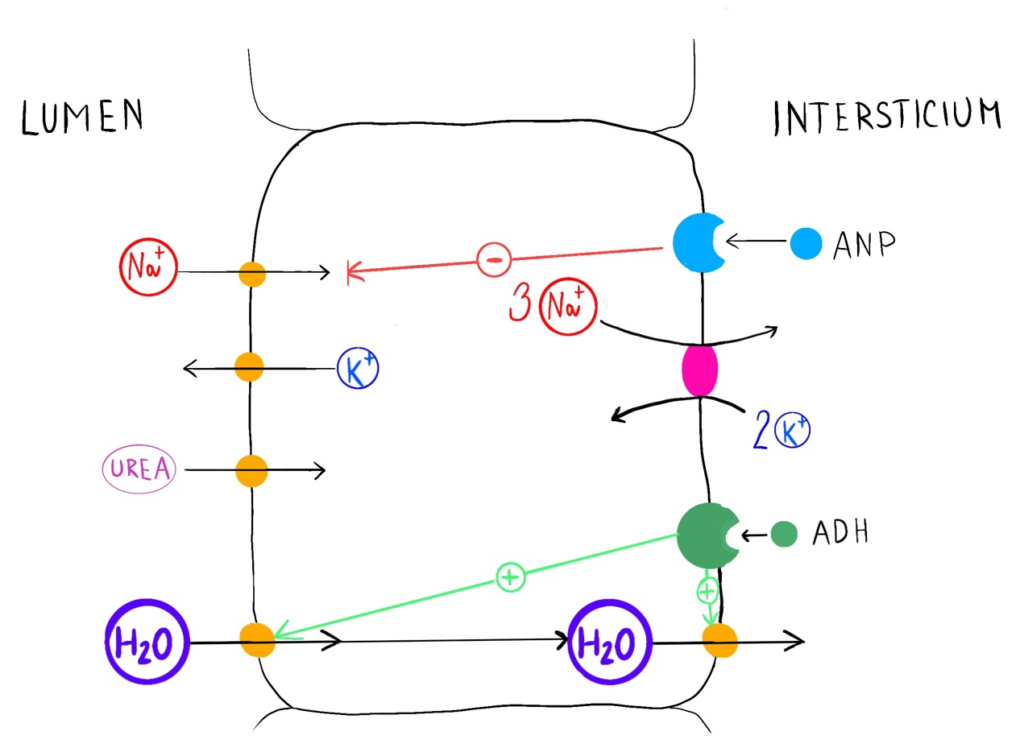
Epitel dřeňových sběrných kanálků.