Epidemiologie – prevalence 2 % (> 75 let života stenóza 4 %, skleróza 50 %), s věkem četnost roste.
Etiologie
- Nejčastěji kalcifikace trojcípé aortální chlopně (degenerativní AS). Typický je vyšší věk pacientů (> 65 let), obtížná předpověď rychlosti progrese vady, vysoká koincidence s ICHS (30 – 50 % pacientů) a polymorbidita pacientů. Typické je, že nejsou srostlé komisury, ale příčinou je rigidita cípů v důsledku jejich kalcifikací. Rizikové faktory shodné s rizikovými faktory aterosklerózy (vysoký LDL cholesterol, lipoprotein a, diabetes mellitus, kouření, chronická nefropatie, metabolický syndrom).
- Bikuspidní aortální chlopeň je druhou nejčastější příčinou AS v dospělosti. Přítomna u cca 2 % populace, manifestuje se ve věku 50 – 65 let života. Důvodem je hemodynamická nevýhodnost dvojcípé chlopně se vznikem turbulencí, které působí zrychlení degenerace. Bikuspidní aortální chlopeň může být součástí komplexní srdeční vady. U postižených jedinců je vyšší incidence koarktace aorty, degenerace medie aorty a tvorba aneuryzmatu ascendentní aorty. Dále byl popsán širší rozměr aorty než při normální trikuspidní aortální chlopni, který je přítomen nezávisle na hemodynamické závažnosti chlopenní vady a je rizikovým faktorem vzniku disekce aorty.
- Revmatická horečka je v současnosti v naší populaci raritní. Revmatický proces je méně agresivní. V řadě případů je je vlastní vada pouze středně významná a až nasedající degenerace vede k progresi ve významnou vadu.
- Radioterapie zaměřená na mediastinum
- Silným patogenetickým faktorem s výrazným familiárním výskytem mohou být určité genetické polymorfismy receptoru pro vitamin D, interleukin 10, apolipoprotein E4 a estrogenový receptor (u postmenopauzálních žen).
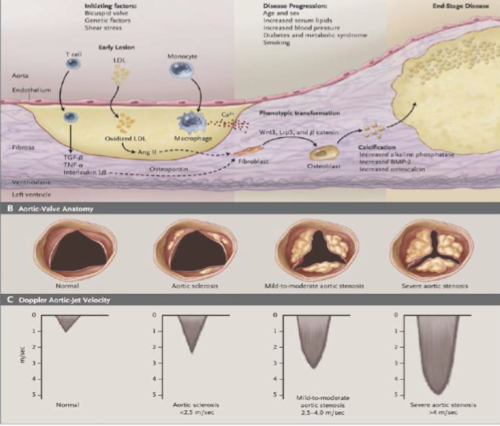
Patofyziologie
- 1. Zúžení na úrovni ústí aorty →
- 2. ↑ tlaková zátěži levé komory a zvýšení afterloadu →
- 3. koncentrická hypertrofie se zvýšením hmotnosti LK (paralelní replikace sarkomer se zmnožením vaziva). Tato adaptace je úvodem hemodynamicky výhodná, protože dochází ke snížení systolického stresu myokardu, přesně jak to popisuje Laplaceuv zákon:
systolický wall stress = (systolický tlak · průměr levé komory) / tloušťka stěny levé komory
Dutina levé komora není zvětšená, ale má větší tloušťku stěn ovšem bez kompenzatorního zvětšení koronárního řečiště s lehkou indukcí ischémie. Zhoršujícím faktorem je snížení hustoty kapilár takto hypertrofovaného myokardu ve srovnání s tloušťkou levé komory, na které dále působí zvýšené kompresní síly při vysokém enddiastolickém tlaku. Tímto mechanismem jsou nejzranitelnější subendokardiální oblasti myokardu. Míra hypertrofie LK je výrazně individuální. Běžná je diastolická dysfunkce.
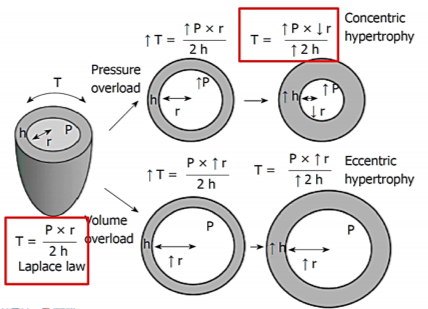
- 4. Velký transaortální tlakový gradient může takto existovat po mnoho roků, aniž by došlo ke snížení minutového objemu nebo dilataci levé komory. Extrémní afterload vede nakonec k systolické dysfunkci LK, která je zpočátku reverzibilní („afterload mismatch“), později ireverzibilní („myopatická fáze“). Následkem je i pokles gradientu levá komora – aorta (a tak i riziko podhodnocení vady) spolu s nárůstem středního tlaku v levé síni, plicnici i pravé komoře. K dalšímu snížení funkce levé komory dochází při současné přítomnosti ICHS, protože hypertrofický myokard má vysoké nároky na dodávku kyslíku.
Nejčastější příčinou vzniku aortální stenózy u dospělých pacientů je degenerace a kalcifikace aparátu aortální chlopně. Patogenetický mechanismus je velmi podobný vaskulární ateroskleróze, včetně endoteliální dysfunkce, akumulace lipidů, aktivace zánětlivých buněk, uvolnění cytokinů a upregulace některých signálních drah. Valvulární myofibroblasty se fenotypově diferencují v osteoblasty s aktivací produkce proteinů kostní matrix a akumulací kalciových krystalů hydroxyapatitu. Dále bylo zjištěno, že aortální skleróza (fokální ztluštění a kalcifikace cípů, které ještě nepůsobí obstrukci) je výrazným rizikovým faktorem infarktu myokardu a syndromu náhlé smrti u osob > 65 let věku.
Při revmatické horečce dochází opět k fúzi komisur, které někdy připomínají bikuspidní chlopeň. Toto predisponuje chlopeň ke traumatizaci, fibróze, kalcifikaci a dalšímu zúžení ústí.
Mimo valvulární stenózu aorty je obstrukce výtokového traktu levé komory přítomna i u supravalvulární aortální stenózy, diskrétní fibromuskulární/membranózní subvalvulární aotální stenózy a hypertrofické obstrukční kardiomyopatii.
CAVE Současná přítomnost mitrální i aortální stenózy (např. po revmatické horečce) snižuje gradient levá komora – aorta a maskuje tedy i typické příznaky aortální stenózy.

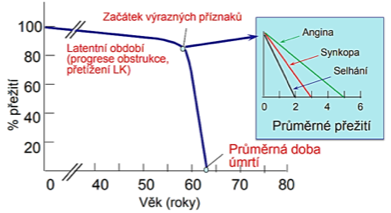
Klinický obraz – aortální stenóza se vyvíjí po řadu let asymptomaticky (zvýšený afterload je kompenzován koncentrickou hypertrofií myokardu a nedochází tedy ke snížení srdečního výdeje) – v tom případě má vynikající prognózu. Symptomatická AS se projevuje typickým trias a jeho prognóza se prudce zhoršuje:
- I. Námahová dušnost – způsobena zvýšením tlaku v plicnici při diastolické dysfunkci levé komory s následným zvýšením enddiastolického tlaku.
- II. Angina pectoris – většinou se projevuje později než dušnost a odráží poruchu rovnováhy mezi zvýšenou potřebou kyslíku v hypertrofickém myokardu a jeho nedostatečnou dodávkou. Situaci dále zhoršuje přítomnost ICHS. Průměrné přežití pacientů po objevení anginy pectoris je 5 let.
- III. Synkopy – vznikají zejména při námaze a jsou většinou způsobeny poklesem arteriálního tlaku díky vazodilataci v pracujících svalech aktivací baroreceptorů v LK při nemožnosti zvýšení srdečního výdeje při zatížení (pro aortální stenózu typické). Dalším mechanismem je snížení srdečního výdeje při rozvoji arytmií. Přežití pacientů po objevení synkopy jsou 3 roky.
V nejpokročilejších stádiích se mohou objevovat příznaky srdečního selhání dopředu (slabost, periferní cyanóza, kardiální kachexie) i dozadu (ortopnoe, paroxysmální noční dyspnoe, plicní edém, fibrilace síní) s přenesením na pravé srdce (hepatomegalie, zvýšená náplň krčních žil, otoky dolních končetin). Průměrné přežití pacientů po objevení srdečního selhání je 2 roky.
Diagnostika
1. Palpace – rytmus bývá až do posledních fází pravidelný a sinusový. V pozdních stádiích se snižuje srdeční výdej i krevní tlak, který narůstá pomalu s opožděným nástupem peaku (pulsus parvus et tardus).
Na jugulární tlakové křivce je u mnoha pacientů zvýšení vlny a, které je způsobeno sníženou roztažností pravé komory, protože se do ní vyklenuje hypertrofické interventrikulární septum. Impuls levé komory bývá dislokován laterálně, při poloze na levém boku je často hmatné jeho zdvojení (hmatná je čtvrtá srdeční ozva S4), na srdeční bázi (napravo od sterna) může být hmatné systolické chvění, zejména při předklonu.
2. Auskultace
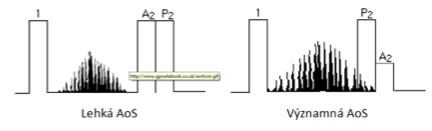
- S2 – jak se vada zhoršuje, může se prodlužovat systola levé komory, takže A2 se postupně přibližuje k P2, poté je s ním synchronní a v pozdních fázích může dokonce za P2 zaostávat (paradoxní rozštěp S2). Zpočátku je slyšitelné normálně, jak cípy kalcifikují, stává se S2 oslabenou.
- S3 – objevuje se v pozdních fázích AS, kdy levá komora již selhává a dilatuje se
- S4 – nejčastěji slyšitelná na hrotu a odpovídá přítomnosti hypertrofie levé komory se zvýšením enddiastolického tlaku levé komory
- při vrozené bikuspidní aortální chlopni bývá u dětí a mladých dospělých slyšitelný protosystolický ejekční zvuk. Při ztluštění, kalcifikaci a imobilizaci cípů aortální chlopně tento zvuk většinou vymizí.
- přítomen hluboký, hrubý, midsystolický (ejekční) šelest, který začíná krátce po S1, na vrcholu ejekce dosahuje svého peaku a končí před S2. Nejjasněji slyšitelný na bázi srdce (nejlépe ve 2. mezižeberním prostoru vpravo) s propagací typicky nahoru podél karotid, příležitostně ale i směrem dolů k hrotu, kde může být zaměněn s šelestem při mitrální regurgitaci (Gallavardiniho efekt). Při těžké obstrukci a zachovalé systolické funkci dosahuje intenzity nejméně III/VI. Při lehké obstrukci, ale i (CAVE) snížené systolické funkci, kdy je srdeční výdej a tedy i transvalvulární tok snížen, má šelest intenzitu nižší.
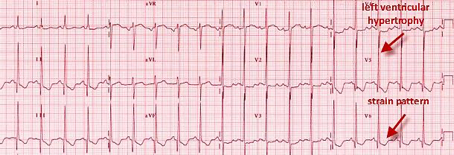
3. EKG – závažnost EKG změn neodpovídá závažnosti hemodynamické závažnosti vady. U většiny pacientů s těžkou aortální stenózou jsou přítomny
- známky hypertrofie levé komory
- známky přetížení levé komory, tedy deprese ST úseku, inverze T („ST strain“) ve svodech I, aVL a V4 – V6
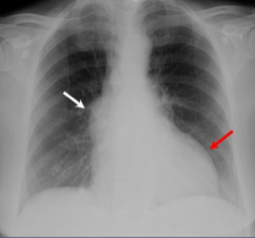
4. RTG S+P – mohou (ale nemusí) být známky mírného zvětšení srdečního stínu. Při dilataci proximální aorty (často při bikuspidní aortální chlopni) může být patrný její stín v předozadní rovině při pravé horní hranici srdce (bílá šipka). Při těžké aortální stenóze jsou patrné téměř pravidelně kalcifikace aparátu aortální chlopně. V dekompenzované fázi bývají srdeční dutiny dilatované s městnáním v plicním řečišti (červená šipka).
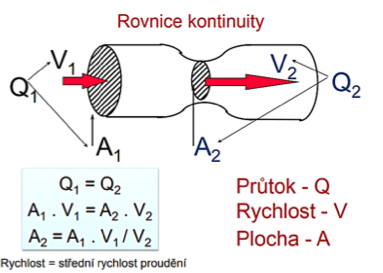
5. Echokardiografie – zásadní metoda. Hodnotí etiologii aortální stenózy, morfologii chlopně (počet cípů, rozsah a lokalizaci kalcifikací) a kvantifikuje významnost vady. Významnost vady je možné stanovit změřením maximálního a středního gradientu na aortálním ústí, lépe pak výpočtem plochy aortálního ústí:
- rovnice kontinuity (plocha aortálního ústí = plocha (LVOT x VTILVOT)/ VTIAo)
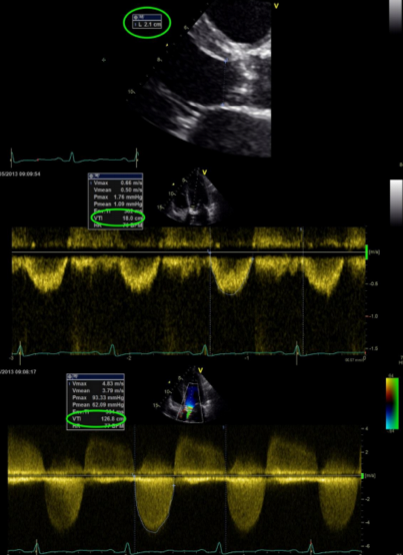
CAVE Určitým úskalím je fenomén restituce tlaku (pressure recovery). U nativních aortálních stenóz se část kinetické energie za vena contracta mění na potenciální energii, tedy tlak, s podhodnocením peakového tlakového gradientu. Tento fenomén je patrný pouze u katetrizační metody stanovení gradientu (většinou klinicky zanedbatelný), u echokardiografie je pomocí CW měřena vždy maximální rychlost, k pressurte recovery tedy nedochází. Toto je důvod, proč je echokardiograficky stanovený gradient vyšší než katetrizační. Vliv pressure recovery je tím vyšší, čím užší je kořen aorty (u dilatovaného kořene aorty je poststenotické zvýšení tlaku nižší, protože se potenciální energie rozloží do většího objemu).

- planimetricky – při dobré vyšetřitelnosti lze AVA změřit přímo z PSAX (u TEE z projekce ME AV SAX).
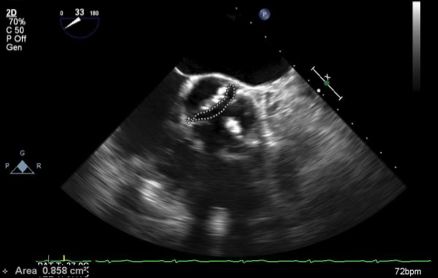
- dobutaminová echokardiografie je indikována při aortální stenóze s nízkým středním gradientem (MG < 40 mm Hg) a nízkou EF LK (< 40 %). Při podání dobutaminu v nízké dávce (< 20 μg/kg/min) se hodnotí vzestup gradientu na aortálním ústí, kontraktilní rezerva (vzestup SV > 20 %) a změnu AVA. Pokud:
- dochází k vzestupu gradientu MG > 40 mmHg při stejné AVA (vzestup o méně než 0,2 cm2), která zůstává pod 1 cm2, jde o pravou těžkou aortální stenózu.
- MG se nemění a AVA stoupá nad 1,2 cm2, jde o tzv. pseudotěžkou aortální stenózu.
- SV se nemění nebo stoupá o < 20 %, jde o těžkou aortální stenózu s vyčerpanou kontraktilní rezervou.

6. Bicyklová ergometrie – indikována u významných vad, které jsou zcela asymptomatické. Pozitivní při vzniku symptomů, poklesu TK nebo jeho vzestupu při zátěži o < 20 mmHg, nemocný nedosáhne 80 % predikované zátěže, vývoji ST depresí pro které není jiné vysvětlení (negativní SKG) a vzniku komplexních komorových arytmií.
CAVE Zátěžové vyšetření je KI u symptomatické vady.
7. Srdeční katetrizace
- SKG je indikována u mužů > 40 let a žen > 45 let (u mladších při podezření na ICHS nebo vrozené vývojové vady koronárních tepen), katetrizace při významné plicní hypertenzi k jejímu rozlišení. Při SKG lze provést i aortografii ke zhodnocení velikosti aorty a semikvantitativně aortální regurgtiace.
- ke kvantifikaci aortální stenózy se katetrizace již rutinně neprovádí, pouze při sporném echo nálezu. Je nutné změřit srdeční výdej, střední gradient (MG), peak-to-peak gradient (PG) na aortálním ústí, a kvantifikovat AVA dle Gorlinovy rovnice:
AVA = CO / (44,3 HR x systolická ejekční perioda x √MG)
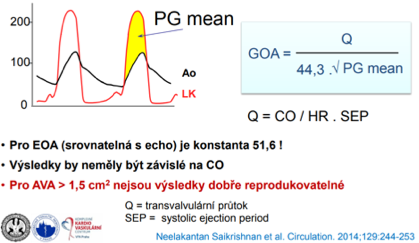
CAVE MG katetrizačně a echokardiograficky dobře koreluje, PG je katetrizačně o cca 20 % nižší než echokardiograficky.
8. CT a CT angiografie – indikováno při patologiích aorty (dilatace, disekce, supravalvární AS, koarktace aorty), před reoperací nebo při úvaze o TAVI. Umožní hodnocení o rozsahu kalcifikací aortální chlopně a srdečních tepen a o velikosti anulu nebo aortálního ústí.
9. BNP, NTproBNP – u pacientů s podezřením na srdeční selhání je vhodné stanovení hladiny BNP. Hodnoty BNP > 70–100 pg/ml mají více než 80% senzitivitu a specificitu k přítomnosti symptomů.
Kvantifikace

Klasická low flow – low gradient aortální stenóza
Nemocní se systolickou dysfunkcí LK (EF < 40 %) mohou mít i při významné vadě (AVAi < 0,6 cm2/m2) střední gradient na aortálním ústí < 40 mmHg. Srdce není schopno vyvinout dostatečnou práci, aby vznikl významný tlakový gradient. U těchto nemocných je užitečné provést dobutaminové UZ vyšetření. Pro významnou vadu svědčí vzestup gradientu a minimální změna AVA (viz výše).
Paradoxní low flow – low gradient aortální stenóza
Existuje i skupina nemocných, kteří mají významnou aortální stenózu (AVA < 1 cm2) a nízký střední gradient (< 40 mmHg) při normální systolické funkci LK. Jedná se o nemocné s nízkým průtokem přes aortální ústí (index tepového objemu, SVi < 35 ml/m2). Tento typ AS se nejčastěji vyskytuje u starších žen s malou, výrazně hypertrofickou LK (koncentrická remodelace) a s anamnézou arteriální hypertenze. Tito pacienti mají těžkou diastolickou dysfunkci LK, sníženou longitudinální funkci při zachované radiální funkci a vysoký podíl fibrózy myokardu. Při podezření na tuto diagnózu je potřeba provést velmi pečlivé echokardiografické vyšetření, případně ho korelovat s katetrizací.
Pseudozávažná aortální stenóza
Degenerativně změněná aortální chlopeň se neotevře díky nízkému SV, který je ale důsledkem primární patologie myokardu (např. ICHS) a nikoliv aortální vady samotné. Rozezná se při dobutaminové echokardiografii, kdy neroste gradient, ale stoupá SV a AVA na hodnoty odpovídající středně závažné aortální stenóze (PG a MG je stejné, stoupá LVOT VTI a tím i AVA).
Terapie aortální stenózy – před každou plánovanou chlopenní intervencí je nutné si vždy položit následující základní otázky:
- Je vada významná?
- Má pacient symptomy? Pokud ano, jsou způsobeny vadou?
- Jaká je životní prognóza pacienta? Jaký je risk:benefit…co pacientovi operace přinese? A jaká jsou přání pacienta?
I. Režimová opatření – při těžké aortální stenóze (AVA < 1 cm2) se nedoporučuje výraznější fyzická námaha. Je nutné se vyvarovat dehydrataci a hypovolémii (snižují srdeční výdej).
II. Farmakoterapie – používá se k potlačení symptomů, při hypertenzi a k léčbě srdečního selhání u inoperabilních pacientů. U plicního edému při těžké aortální stenóze lze podat opatrně nitráty, opatrně diuretika, digoxin, ACEI nebo sartany.
CAVE
- Medikamentózní léčba AS neovlivňuje životní prognózu.
- Důležité je udržení sinusového rytmu.
- Hypovolémie a ↓ preloadu může vést u malé LK ke ↓ MAP a CO.
- Léčba statiny nezpomaluje progresi AS.
III. Chirurgická terapie – AVR by měla být indikována:
- u všech pacientů se symptomatickou těžkou aortální stenózou (u středně těžké vady při současně prováděné kardiochirurgické operaci z jiné indikace). U paradoxní low flow – low gradient po pečlivém ověření závažnosti vady.
- při poklesu systolické funkce levé komory (EF LK < 50 %)
- při pozitivním zátěžovém testu
- u low flow low gradient po průkazu kontraktilní rezervy (lze zvážit i u jedinců bez průkazu kontraktilní rezervy
- u asymptomatických při Vmax > 5,5 m/s nebo při progresi > 0,3 m/s/rok.
- lze zvážit i u asymptomatických jedinců s nízkým chirurgickým rizikem při významném zvýšení natriuretických peptidů bez jiné vysvětlující příčiny, zvýšení MP < 20 mmHg při zátěžovém testu, při masivní hypertrofii levé komory.
Vzhledem k morfologickým změnám je nutná náhrada chlopně, nikoliv její rekonstrukce. Výjimkou je kongenitální AS, kdy lze provést discizi komisur aortální chlopně. I tyto chlopně ale později dospějí do stadia postižení, kdy bude nezbytná jejich náhrada. Operace probíhá za použití mimotělního oběhu a v kardioplegické srdeční zástavě (nejčastěji studená krevní kardioplegie). Standardním přístupem je mediální sternotomie. V posledním období se zvyšuje snaha chirurgů o miniinvazivní přístup – náhradu aortální chlopně z ministernotomie nebo krátké pravostranné torakotomie. Základní otázkou je volba umělé chlopně.
- Mechanické chlopně mají vynikající hemodynamické vlastnosti (na principu dvoulistých chlopní). Riziko mechanického selhání je prakticky nulové. Základní požadavkem je nutnost doživotní antikoagulační léčby v pečlivě sledovaném terapeutickém rozmezí INR 2,0–3,0. Nedostatečná antikoagulační léčba ohrožuje nemocného blokací chlopně trombózou. Doposud se používá warfarin.
- Biologické chlopně (bioprotézy) jsou vyrobeny z biologické tkáně, upevněné na podpůrné konstrukci (stentu). Nejčastěji se používají chlopně vyrobené z bovinního perikardu, méně často prasečí aortální chlopně. Implantace bioprotézy je obdobná jako u mechanických chlopní. Hemodynamické vlastnosti jsou výborné, ale plocha efektivního ústí u malých velikostí, potřebných v případě úzkého aortálního anulu, je poněkud menší než u chlopní mechanických. Základní výhodou je absence nutnosti antikoagulační léčby. Doporučená je pouze antiagregační medikace ASA. Nevýhodou je nejistota dlouhodobé trvanlivosti. Rychlost rozvoje degenerativních změn je ovlivněna věkem příjemce; s vyšším věkem se výrazně zpomaluje. Od určité věkové hranice je potom předpokládaná doba dobré funkce bioprotézy srovnatelná s předpokládanou vyhlídkou doby života. Obecná shoda panuje na věku okolo 70 let (nyní se posouvá do 65 let). Před náhradou aortální chlopně ve věkově „šedé“ zóně je nutný podrobný rozhovor s nemocným a respektování jeho osobních preferencí.
- Aortální homograft (kadaverózní lidský aortální kořen) je další možnou náhradou aortální chlopně. Odběr, příprava a uchování (kryoprezervace při –190°C) je programovou činností tkáňové banky. Ve spolupráci s ní lze pro konkrétního pacienta připravit, na operačním sále rozmrazit a použít aortální homograft vhodné velikosti, předem určené pomocí předoperačního echokardiografického vyšetření. Implantace homograftu je technicky náročnější než u mechanické nebo biologické umělé chlopně. Metodou implantace je náhrada celého aortálního kořene in toto (root replacement. Koronární tepny je nutno reimplantovat do homograftu. Homograft nevyžaduje antikoagulaci, ale podléhá degeneraci a kalcifikaci obdobně jako umělé bioprotézy. Hlavní výhodou je zvýšená odolnost proti infekci. Hlavní indikací pro implantaci aortálního homograftu je pokročilá aortální endokarditida s přechodem infekce do aortálního anulu (abscesy).
- Rossova operace je výkonem, kdy je aortální chlopeň včetně celého kořene nahrazena vlastním plicnicovým kořenem daného nemocného (autograftem). Kontinuita pravostranného tepenného výtoku je potom obnovena pomocí plicnicového homograftu (kadaverózního). Jde o technicky rozsáhlý chirurgický výkon, který má ale významnou výhodu, a to že není potřeba chronická antikoagulační léčba a navíc umožňuje vysokou kvalitu života. Nevýhodou je vyšší operační riziko a „ohrožení dvou chlopní: nová aortální chlopeň (možný pozdní vývoje regurgitace) a plicnicový homograft, který je často nutné reoperovat pro vznik kalcifikací. Výkon je ale pro svou rozsáhlost spojen s vyšším operačním rizikem a v dlouhodobém horizontu staví do rizika dvě chlopně: „neo-aortální“ (možný pozdní vývoj regurgitace na plicnicovém autograftu) i plicnicový homograft, který bude nutno v určitém procentu v pozdním období reoperovat – vyměnit pro vznik degenerativních kalcifikací.
- AS (obdobně jako AR) může být spojena s dilatací vzestupné aorty. V závislosti na morfologii aortální dilatace je chirurgickým řešením náhrada chlopně a izolovaná suprakoronární náhrada vzestupné aorty (je-li kořen normální a dilatace začíná až nad sinotubulární junkcí) nebo implantace kompozitního konduitu – cévní protézy osazené na proximálním konci mechanickou nebo biologickou chlopenní protézou (postihuje-li dystrofická dilatace aortální kořen i vzestupnou aortu – Bentallova operace). V takovém případě je nutno reimplantovat ústí koronárních tepen do cévní protézy.
Nyní narůstá snaha o co nejmenší invazivitu…výkony prováděné z krátké sternotomie nebo pravostranné torakotomie se zavedením bezstehové, samoexpandabilní protézy (podobné TAVI). Prognóza AVR je dobra. Operační mortalita AVR je 3 %, AVR + CABG 4,5 %. Samozřejmě závisí na EuroSCORE II: http://www.euroscore.org/calc.html
IV. Katetrizační léčba
Balónková valvuloplastika je používána jako:
- dočasné řešení vrozených AS v dětském věku nebo adolescenci (při příznivé morfologii chlopně, bez kalcifikací a bez AR větší než 1. stupně). Většina pacientů po balonkové valvuloplastice provedené v dětství vyžaduje v dospělosti operaci pro restenózu nebo progresi AR.
- paliativní výkon u pacientů tak rizikových, že nejsou schopni ani TAVI
- dočasné řešení u hemodynamicky nestabilních pacientů jako most k dalšímu řešení
V dospělosti se jedná o poměrně rizikový výkon (komplikace v cca 10 %) s jen přechodnou úlevou. Po 6–12 měsících dochází k restenóze a ke klinickému zhoršení.
CAVE Balonková valvuloplastika sama o sobě nezlepšuje přežití nemocných.
Gradient na aortální chlopni bývá po balonkové valvuloplastice redukován o cca o 50 % a AVA se zvětší cca o 25 %. U bikuspidních aortálních chlopní jsou výsledky horší.
V. TAVI – při EuroSCORE II > 20 % (to ale nadhodnocuje, lepší je STS >10 % http://riskcalc.sts.org/stswebriskcalc/#/calculate) je TAVI dobrou alternativou s úspěšností > 90 % (30 denní mortalita 5 – 15 %, jednoletá mortalita 20 – 40 %). Komplikace:
- cévní mozková příhoda (1–5 %)
- nutnost zavedeni kardiostimulátoru (do 7 % u chlopně roztažitelné, do 40 % u samoexpandibilni chlopně)
- cévní komplikace (do 20 %)
- často paravalvulární regurgitace (obvykle mírná)
Pro TAVI nevhodné situace jsou porcelánová aorta, stav po ozáření hrudníku, průchodné aortokoronární bypassy aj. Poslední slovo má vždy kardiotým.
Absolutními kontraindikacemi TAVI jsou přepokládaná délka života < 1 rok, popř. nemožnost zlepšení kvality života, současný kardiochirurgický výkon na jiných chlopních. Dále trombus v levé komoře, aktivní endokarditida, aortální anulus < 19 mm resp. > 29 mm, riziko obstrukce koronárních ústí (např. malá vzdálenost anulu a koronárních sinusů).
Follow-up
- Symptomatičtí pacienti – rychlé chirurgickému řešení.
- Asymptomatičtí s významnou AS – TTE + zátěžové vyšetření á 6 měsíců.
- Asymptomatičtí se středně významnou AS – TTE + zátěžové vyšetření á 12 měsíců. Při vyvolání symptomů → operace.